某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是:
 |
| A.含有大量SO42-的溶液中肯定不存在Ag+ |
| B.Ag2SO4的溶度积常数(Ksp)为1×10-4 |
| C.0.02mol/L的AgNO3溶液与0.2mol/L的Na2SO4溶液等体积混合不会生成沉淀 |
| D.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
下列操作方法或实验装置正确的是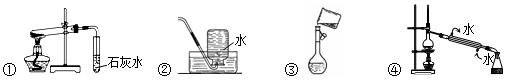
| A.装置①探究NaHCO3的热稳定性 | B.装置②SO2的收集 |
| C.装置③向容量瓶中转移液体 | D.装置④石油蒸馏 |
下列变化中,属于加成反应的是
| A.乙烯使酸性KMnO4溶液褪色 | B.将苯滴入溴水中,振荡后水层接近无色 |
| C.乙烯使溴的四氯化碳溶液褪色 | D.甲烷与氯气混合光照一段时间后黄绿色消失 |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,48 g O3含有的氧原子数均为3NA |
| B.常温常压下,11.2 L乙烯(C2H4)含有2NA个碳原子 |
| C.1.7 g氨气所含有的电子数目为10 NA |
| D.71g氯气与足量氢氧化钠溶液反应转移的电子数2NA |
将下列物质按酸、碱、盐分类排列,正确的是
| A.硫酸纯碱硫酸钙 | B.氢氯酸烧碱硫酸亚铁 |
| C.碳酸乙醇烧碱 | D.磷酸熟石灰苛性钠 |
将SO2通入BaCl2溶液中至饱和未见有沉淀生成,继续加入另一物质,仍无沉淀生成,则该物质可能为
| A.Cl2 | B.NH3 | C.H2SO4 | D.HCl |