(每空2分,共14分)
中国是《日内瓦协定书》的缔约国,一贯反对使用化学武器,反对任何形式的化学武器扩散,苯氯乙酮是一种具有荷花香味且具有强催泪作用的化学毒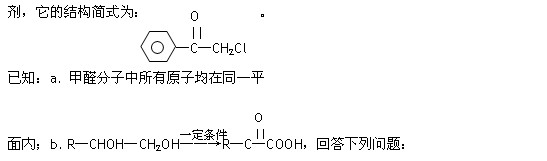
(1)苯氯乙酮分子中,在同一平面内的碳原子最多有 个。
(2)苯氯乙酮不可能发生的化学反应是 。
| A.加成反应 | B.取代反应 | C.消去反应 | D.水解反应 E.银镜反应 |
(3)分子中有苯环但不含甲基,且能发生银镜反应的苯氯乙酮的同分异构体有 种。
(4)苯氯乙酮的一种同分异构体有下列转化关系: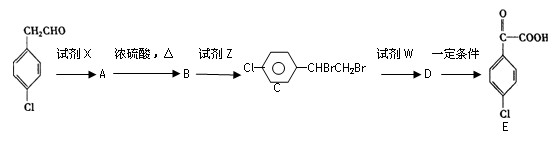
请写出:
①B的结构简式: ,试剂X为 。
②下列转化的化学方程式A→B ;
A+E→F ;
某二元弱酸H2A溶液,按下式发生一级和二级电离:
H2A H++HA-
H++HA-
HA- H++A2-
H++A2-
已知相同浓度时H2A要比HA-的电离能力强,即:K1>>K2。设有下列四种溶液:
A.0.01mol.L-1的H2A溶液
B.0.01mol.L-1的NaHA溶液
C.0.01mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
D.0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
c(H+)最大的是___________,最小的是 。
c(H2A)最大的是_____________,最小的是__________。
c(A2-)最大的是______________,最小的是___________。
把AlCl3(aq)蒸干灼热,最后得到的固体产物是什么?(用化学方程式表示,并配以必要的文字说明) 。
氯气有毒,一旦泄露会造成对空气的严重污染。工业上常用浓氨水检验氯气管是否漏气。(已知Cl2可将NH3氧化成N2)请简要说明这种检验方法的依据:
。并写出有关反应的化学方程式为。
肼(N2H4)是火箭推进剂的成分之一,它与另一成分NO2反应生成N2和H2O,反应的化学方程式为,其中氧化剂是,该反应除产生大量的热量外,还有一突出的优点是.
锌与硝酸反应,若有1mol硝酸参加法院,则有0.8mol的电子发生转移,此时硝酸的还原产物中N元素的化合价 。