2009年12月7日~18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议,大会倡导“节能减排”和“低碳经济”的绿色环保主题,中国宣布了2020年二氧化碳排放量下降40~45%的减排目标。下列不符合这一主题的是( )
| A.自备购物布袋,不用塑料方便袋 |
| B.开发新能源,如太阳能、风能等,减少对化石能源的依赖 |
| C.推广煤的气化、液化技术,提供清洁燃料和化工原料 |
| D.给汽车安装尾气处理器 |
将11.9 g Mg、Al、Fe组成的合金溶于足量NaOH溶液中,产生的气体在标准状况下体积为3.36 L。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀19.4 g,则上述反应中生成NO气体的体积为(标准状况下)
| A.6.72 L | B.11.2 L | C.22.4 L | D.4.48 L |
汽车上的催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:
2NO(g)+2CO(g) N2(g)+2CO2(g)DH=-a kJ/mol(a>0)
N2(g)+2CO2(g)DH=-a kJ/mol(a>0)
在某温度时,用气体传感器测得不同时间的NO和CO浓度如下表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| c(NO)/10-4 mol·L-1 |
10.0 |
4.05 |
2.50 |
1.60 |
1.00 |
1.00 |
| c(CO)/10-3 mol·L-1 |
3.60 |
3.05 |
2.85 |
2.76 |
2.70 |
2.70 |
经分析,得出结论不正确的是
A.2~3s间的平均反应速率v(NO)=9×10-5 mol/(L·s)
B.催化转化器对废气的转化速率在夏季时比冬季时高
C.若该催化转化器气舱容积为2L,则达到平衡时反应放出热量1.8a J
D.该温度下,此反应的平衡常数K=5000
25℃时,水溶液中c(H+)与c(OH-)的变化关系如图中曲线a c所示,下列判断错误的是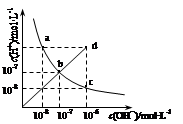
| A.a c曲线上的任意一点都有c(H+)·c(OH-)=10-14 |
| B.b d线段上任意一点对应的溶液都呈中性 |
| C.d点对应溶液的温度高于25℃,pH<7 |
| D.CH3COONa溶液不可能位于c点 |
下列实验操作能达到目的的是
| A.除去苯中混有的少量苯酚:加入适量NaOH溶液,振荡、静置后分液 |
| B.除去乙酸乙酯中混有的少量乙酸:加入NaOH溶液并加热,振荡、静置后分液 |
| C.检验卤代烃中的卤原子:取少量液体与NaOH溶液共热后滴加AgNO3溶液 |
| D.检验FeCl3溶液中是否含有Fe2+:取少量溶液先滴加氯水,再滴加KSCN溶液 |
某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4==2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是
| A.乙烧杯中发生还原反应 |
| B.甲烧杯中溶液的pH逐渐减小 |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.外电路的电流方向是从a到b |