A、B、C、D、E 是同一短周期的五种元素, A和B的最高价氧化物对应的水化物呈碱性, 且碱性前者强于后者, C和D的气态氢化物的水溶液呈酸性, 且酸性前者强于后者, 五种元素形成的简单离子中,E的离子半径最小, 则它们的原子序数由大到小的顺序是
A. BADCE B. ECDAB C. BAEDC D. CDEBA
下列装置或操作能达到实验目的的是
NA表示阿伏加德罗常数,下列说法中正确的有
①20 g D2O含有的电子数为10NA②常温下,4 g CH4含有NA个C-H共价键
③10 mL质量分数为98%的H2SO4,加水至100 mL,H2SO4的质量分数为9.8%
④标准状况下,5.6L四氯化碳含有的分子数为0.25NA
⑤25 ℃时,pH=12的1.0 L CH3COONa溶液中水电离出的OH-的数目为0.01NA
⑥1 mol Na2O2与水完全反应时转移电子数为2NA
| A.5个 | B.2个 | C.3个 | D.4个 |
下列关于氯的说法正确的是
| A.Cl2在化学反应中既能作氧化剂,又能作还原剂 |
| B.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| C.Cl2通入到含有酚酞的NaOH溶液中,红色褪去,因为氯气有漂白性 |
| D.将SO2通入次氯酸钙溶液可生成次氯酸 |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到直观形象
的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物: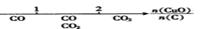 |
B.Fe在Cl2中的燃烧产物: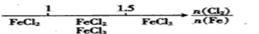 |
C.向AlCl3溶液中滴加NaOH后铝的存在形式: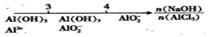 |
D.氨水与SO2反应后溶液中的铵盐: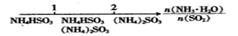 |
将下图所示实验装置的K闭合,下列判断错误的是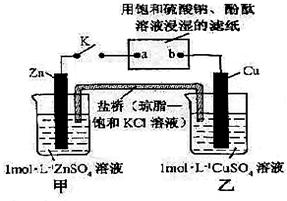
| A.盐桥中的K+移向乙池 |
B.电子沿Zn a a b b Cu路径流动 Cu路径流动 |
| C.b电极上的反应式为4OH-—4e-=O2↑+2H2O |
| D.片刻后可观察到滤纸a点变红色 |