在下列有关晶体的叙述错误的是( )
| A.离子晶体中,一定存在离子键 | B.原子晶体中,只存在共价键 |
| C.离子晶体中可能存在共价键 | D.分子晶体中有可能存在离子键 |
乙酸分子的结构式为 ,下列反应及断键部位正确的是()
,下列反应及断键部位正确的是()
(1)乙酸的电离,是①键断裂
(2)乙酸与乙醇发生酯化反应,是②键断裂
(3)在红磷存在时,Br2与CH3COOH的反应:CH3COOH+Br2 CH2Br—COOH+HBr,是③键断裂
CH2Br—COOH+HBr,是③键断裂
(4)乙酸变成乙酸酐的反应:2CH3COOH―→  +H2O,是①②键断裂
+H2O,是①②键断裂
| A.仅(1)(2)(3) | B.(1)(2)(3)(4) |
| C.仅(2)(3)(4) | D.仅(1)(3)(4) |
下列反应中,属于取代反应的是()
①CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH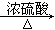 CH2=CH2↑+H2O
CH2=CH2↑+H2O
③CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3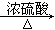 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |
可用来鉴别乙烯、甲苯、乙酸乙酯、乙醇溶液的一组试剂是()
| A.溴水、氯化铁溶液 |
| B.溴水、酸性高锰酸钾溶液 |
| C.溴水、碳酸钠溶液 |
| D.氯化铁溶液、酸性高锰酸钾溶液 |
将1 mol乙醇(其中的氧用18O标记)在浓硫酸存在的条件下与1 mol乙酸充分反应,下列叙述不正确的是()
| A.生成的乙酸乙酯中含有18O |
| B.生成的水分中含有18O |
| C.可能生成88 g乙酸乙酯 |
| D.不可能生成88 g乙酸乙酯 |
实验室用乙酸、乙醇、浓硫酸制取乙酸乙酯,加热蒸馏后,在饱和Na2CO3溶液上面得到无色油状液体,当振荡混合时,有气泡产生,原因是()
| A.产品中有被蒸馏出的H2SO4 |
| B.有部分未反应的乙醇被蒸馏出来 |
| C.有部分未反应的乙酸被蒸馏出来 |
| D.有部分乙醇跟浓硫酸作用生成CO2 |