根据相关化学原理,下列判断正确的是( )
A.若X是原子晶体,Y是分子晶体,则熔点:X<Y
B.若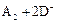 ═
═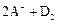 ,则氧化性:D2>A2
,则氧化性:D2>A2
C.若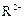 和
和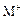 的电子层结构相同,则原子序数:R<M,离子半径:
的电子层结构相同,则原子序数:R<M,离子半径: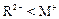
D.若弱酸HA、HB的酸性HA>HB,则溶液的碱性NaA>NaB
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
| A.c(H+) | B.K电离(HF) |
| C.c(F-)/c(H+) | D.c(H+)/c(HF) |
下图表示反应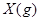

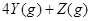 ,
,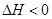 ,在某温度时
,在某温度时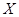 的浓度随时间变化的曲线:
的浓度随时间变化的曲线: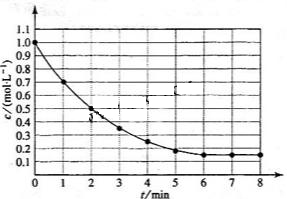
下列有关该反应的描述正确的是
A.第6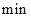 后,反应就终止了 后,反应就终止了 |
B.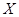 的平衡转化率为85% 的平衡转化率为85% |
C.若升高温度,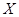 的平衡转化率将大于85% 的平衡转化率将大于85% |
| D.若降低温度,v正和v逆将以同样倍数减少 |
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g) 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
A.该反应的化学平衡常数表达式是K=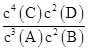 |
| B.此时,B的平衡转化率是40% |
| C.增大该体系的压强,化学平衡常数增大 |
| D.增加B,B的平衡转化率增大 |
在5 L的密闭容器中,一定条件下发生化学反应:2NO(g)+2CO(g) N2(g)+2CO2(g)。起始反应时NO和CO各为3,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
N2(g)+2CO2(g)。起始反应时NO和CO各为3,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
| A.达到平衡后,若将容器体积压缩为2 L,则正反应速率将增大,逆反应速率将减小 |
| B.反应前5秒钟内,用CO表示的平均反应速率为0.04 mol·L-1·s-1 |
| C.当v正(CO)=2v逆(N2)时,该反应中NO的物质的量不再改变 |
| D.保持压强不变,往容器中充入1 mol He,正、逆反应速率都不改变 |
下列事实中,不能用勒夏特列原理解释的是
| A.开启啤酒后,瓶中马上泛起大量泡沫 |
| B.钢铁在潮湿的空气中容易生锈 |
| C.实验室中常用排饱和食盐水的方法收集氯气 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |