用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是

| A. | 上下移动①中铜丝可控制 的量 |
| B. | ②中选用品红溶液验证 的生成 |
| C. | ③中选用 溶液吸收多余的 |
| D. | 为确认 生成,向①中加水,观察颜色 |
已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),如下图,则下列判断错误的是 ( )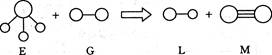
| A.G是最活泼的非金属单质 | B.L是极性分子 |
| C.E能使紫色石蕊试液变蓝色 | D.M化学性质活泼 |
下列有关说法中,不正确的是()
| A.离子晶体的晶格能越大,离子晶体的熔点越高 |
| B.碘单质在水中溶解度很小,但在CCl4中溶解度很大,这是因为CCl4和I2都是非极性分子,而H2O是极性分子 |
| C.成键原子的原子轨道重叠越多,共价键越牢固 |
| D.含有金属阳离子的晶体一定是离子晶体 |
下面叙述正确的是 ( )
| A.共价化合物中没有离子键 |
| B.离子化合物中没有共价键 |
| C.正四面体构型的分子,键角均为109°28' |
| D.直线型分子中的键角均为180° |
下列说法正确的是(NA为阿伏加德罗常数的值( )
| A.124g P4含有的P-P键的个数为4NA |
| B.12 g石墨中含有C-C键的个数为2NA |
| C.12g金刚石中含有C-C键的个数为2NA |
| D.60g SiO2中含Si-O键的个数为2NA |
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是()
A.元素A、B组成的化合物常温下一定呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
C.工业上常用电解D的氯化物制备D
D.化合物AE与CE有相同类型的化学键