下列做法不能体现低碳生活的是
| A. | 减少食物加工过程 | B. | 注意节约用电 |
| C. | 尽量购买本地的、当季的食物 | D. | 大量使用薪柴为燃料 |
下列是一些同学学习“化学反应速率和化学平衡”专题后,联系工业生产实际所发表的观点,你认为不正确的是
| A.怎样在一定时间内快出产品是运用了化学反应速率理论 |
| B.怎样使用有限原料多出产品是运用了化学平衡理论 |
| C.怎样提高原料转化率是运用了化学反应速率理论 |
| D.怎样使原料尽可能多地转化为产品是运用了化学平衡理论 |
下列溶液中加入少量NaOH固体导电能力变化不大的是
| A.盐酸 | B.CH3COOH | C.NH3·H2O | D.H2O |
下列说法正确的是
| A.某一反应的活化分子百分数是个定值 |
| B.升高温度会加快化学反应速率,其原因是增加了活化分子百分数 |
| C.活化分子之间发生的碰撞一定为有效碰撞 |
| D.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子百分数,从而使反应速率增大 |
中国已经成为全球最大轿车生产国,汽车尾气正成为城市的主要空气污染源。NO和CO都是汽车尾气中的有害物质,它们能缓慢反应生成N2和CO2,为控制汽车污染有人提出以下建议,你认为合理的是
| A.增大压强 | B.使用催化剂 |
| C.降低压强 | D.升高反应温度加快反应速率 |
在一定温度下,可逆反应A(g) + 3B(g)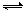 2C(g) 达到平衡的标志是
2C(g) 达到平衡的标志是
A.A、B、C的浓度不再变化
B.A、B、C的分子数之比为1 ∶3 ∶ 2
C.C生成的速率与A生成的速率相等
D.单位时间生成n mol A,同时生成3n mol B