短周期元素形成的常见非金属固体单质与常见金属单质,在加热条件下反应生成化合物,与水反应生成白色沉淀和气体,既能溶于强酸,也能溶于强碱。在足量空气中燃烧产生刺激性气体,在大气中能导致酸雨的形成。被足量氢氧化钠溶液吸收得到无色溶液。溶液在空气中长期放置发生反应,生成物之一为。与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质的元素位于周期表中第周期,第族。
(2)与氢氧化钠溶液反应的化学方程式为:。
(3)与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为,当生成2二氧化氯时,转移电子。
(4)溶液在空气中长期放置生成的化学反应方程式为:。
(5)的溶液与稀硫酸反应产生的现象为。
从氧化还原反应的角度看
(1)在制备下列三种气体时,盐酸起什么作用:(填序号)
①制备H2 Zn + 2HCl =ZnCl2 + H2 ↑盐酸起作用
②制备Cl2 MnO2 + 4HCl = MnCl2 + 2H2O + Cl2↑ 盐酸起作用
③制备CO2 CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 盐酸起作用
| A.氧化剂 | B.还原剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂也不是还原剂 |
(2)氮氧化物对大气的最大的破坏作用之一是能促使臭氧分解,破坏臭氧层:2O3NOx3O2,该反应是否属于氧化还原反应?(填“是”或“不是”),简述理由。
无机化合物可根据其组成和性质进行分类:
(1)上述所示的物质分类方法名称是。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面。(各空填写一个化学式即可)
| 物质类别 |
酸 |
碱 |
盐 |
氧化物 |
氢化物 |
| 化学式 |
① HCl ② |
③ ④Ba(OH)2 |
⑤Na2CO3 ⑥ |
⑦ CO2 ⑧ Na2O |
⑨ NH3 ⑩H2O |
(3)写出⑦转化为⑤的化学方程式:。
(4)写出①与③反应的离子方程式:。
右图为以惰性电极进行电解: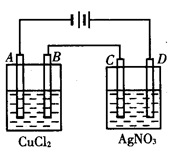
(1)写出B、C、D各电极上的电极反应式和总反应方程式:
A:________________________________,
B:________________________________,
总反应方程式:________________________;
C:________________________________,
D:________________________________,
总反应方程式:___________________________;
(2)在A、B、C、D各电极上析出生成物的物质的量比为__________________。
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: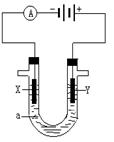
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为___________________________,在X极附近观察到的现象是:__________________。
(2)Y电极上的电极反应式是_________,检验该电极反应产物的方法是:____________________________________。
(3)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是_________,电极反应式是________________,Y电极的材料是_________,电极反应式是__________________。
(1)Cu(NO3)2的水溶液呈(填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示):;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以(填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈性,原因是(用离子方程式表示):______,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的。