I下列描述中正确的是()
| A. | 为 形的极性分子 |
| B. | 的空间构型为平面三角形 |
| C. | 中有6对完全相同的成键电子对 |
| D. | 和 的中心原子均为 杂化 |
Ⅱ金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)原子的核外电子排布式为;
(2)、的晶体结构类型均与氯化钠的相同,和的离子半径分别为69和78 ,则熔点(填"<"或">");
(3)晶胞中和的配位数分别为、;
(4)金属镍与镧()形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为;


(5)丁二酮肟常用于检验:在稀氨水介质中,丁二酮肟与反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是键,碳氮之间的共价键类型是,氮镍之间形成的化学键是;
②该结构中,氧氢之间除共价键外还可存在;
 ③该结构中,碳原子的杂化轨道类型有。
③该结构中,碳原子的杂化轨道类型有。
已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。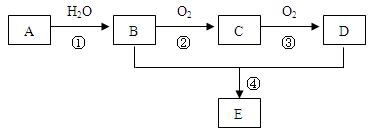
请回答下列问题:
(1)写出A的结构简式。
(2)B、D分子中的官能团名称分别是 、。
、。
(3)物质B可以被直接氧化为D,需要加入的试剂是。(4)写出下列反应的化学方程式:
①;
反应类型:。
④。
反应类型:。
在盛有少量无水乙醇的试管中,加入一小块新切的、擦干表 面煤油的金属钠,迅速用配有导管的单孔塞塞住试管口,用一小试管收集并验纯气体后,点燃,并把干燥的小烧杯罩在火焰上,片刻,迅速倒转烧杯,向烧杯中加入少量澄清石灰水。
面煤油的金属钠,迅速用配有导管的单孔塞塞住试管口,用一小试管收集并验纯气体后,点燃,并把干燥的小烧杯罩在火焰上,片刻,迅速倒转烧杯,向烧杯中加入少量澄清石灰水。
观察现象,完成下表。
| 乙醇与钠反应的现象 |
气体燃烧的现象 |
检验产物 |
| 气体燃烧时火焰呈, 小烧杯内壁, 澄清石灰水。 |
反应中只生成了 |
写出乙醇与钠反应的化学方程式

重要的化工原料F(C5H8O4)有特殊的香味,可通过以下流程合成: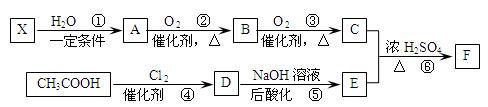
已知:①X是石油裂解气主要成分之一,与乙烯互为同系物;
②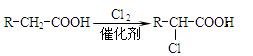 ;
;
③C、E、F均能与NaHCO3反应生成气体。
(1)X加聚产物的结构简式是;
(2)D中所含官能团的名称是;
(3)反应②的化学方程式为,反应类型是;
反应⑥的化学方程式为;
(4)F的同分异构体很多,其中一种同分异构体只含有一种官能团,在酸性或碱性条件下都能水解生成两种有机物,该同分异构体的结构简式是。
在一次兴趣小组活动中,一小组利用物质间的互变,设计成一平面“魔方”如图所示。已知: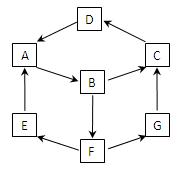
①A、B、C、D、G含有同种元素。
②E是通常情况下密度最小的气体;B与硝酸银溶液反
应生成不溶于稀硝酸的白色沉淀;B也能将一种能形成酸
雨的氧化物氧化为F,F是一种含氧酸,且F的稀溶液
能与A反应生成E和G。
| 物质 |
纯A(单质) |
B(溶液) |
D(固体) |
G(溶液) |
| 颜色 |
银白色 |
黄色 |
红棕色 |
浅绿色 |
③几种物质的部分物理性质:
依据以上信息填空:
(1)G生成C的过程中所出现的现象为;
(2)写出下列反应的化学方程式:
A→B :;
(3)写出下列反应的离子方程式:
B→F:;
酸性条件下,G与次氯酸溶液反应:;
(4)使一定质量的Zn与100mL18.5 mol·L-1酸F的浓溶液充分反应,Zn完全溶解,同时生成标准状况下的气体A 33.6L。将反应后的溶液稀释至1L,测得溶液中c(H+)=0.1mol·L-1,则气体A的成份及体积比为。
现有A、B、C、D、E五种原子序数依次增大的短周期元素,其中在所有的短周期元素中,A的原子半径与D的原子半径之比最小(不包括稀有气体),C与A、B、D均能形成多种常见化合物,B元素的最高价氧化物对应的水化物与其氢化物反应生成一种盐,化合物AE常温下为气体。回答下列问题:
(1)A分别与B、C形成的最简单化合物中,稳定性>(用分子式表示),其中A与B形成的最简单化合物分子的空间构型为;
(2)化合物甲、乙均是由上述五种元素中的三种组成的强电解质,且常温下两种物质的水溶液pH均大于7,组成元素的原子数目比均为1∶1∶1,其中乙是某种家用消毒液的有效成分,则化合物甲的电子式为。
(3)化合物丙由C和D两种元素组成,其中C和D的原子个数比为1∶1,则丙中含有的化学键类型是;
(4)B元素的最高价氧化物对应的水化物与其氢化物反应生成的盐的水溶液呈性(填“酸”、“碱”或“中”),用离子方程式解释原因;
(5)写出实验室制取单质E的离子方程式是。