根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是( )
| A.3 | B.4 | C.5 | D.6 |
下列装置或操作能达到实验目的的是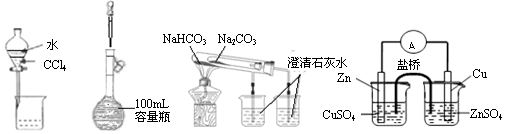
| A.分离水和CCl4 | B.定容 | C.比较两种盐的热稳定性 | D.构成铜锌原电池 |
下列试剂不能鉴别己烯、丙醛和苯酚溶液的是
| A.银氨溶液 | B.FeCl3溶液 | C.新制氢氧化铜悬浊液 | D.酸性高锰酸钾溶液 |
下列大小顺序排列完全正确的组合是
| A.气态氢化物的稳定性:HF>NH3>PH3>H2S |
| B.沸点:苯酚>CH3OH>HCHO>CH3COOH |
| C.离子半径:S2->O2->F- |
| D.相同温度、相同浓度溶液中水的电离程度:NH4Cl>CH3COOH>HCl>Ba(OH)2 |
某溶液灼烧时,透过蓝色钴玻璃未见到紫色火焰,下列判断中错误的是
| A.该溶液中一定不含钾元素 | B.该溶液中不可能含钠的化合物 |
| C.该溶液中不可能含钠单质 | D.该溶液中可能含钠的化合物 |
下列物质的化学用语正确的是
A.二氧化碳的电子式: |
B.次氯酸的结构式:H—Cl—O |
C.甲烷分子的球棍模型: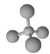 |
D.S2-的离子结构示意图: |