下列离子方程式正确的是
| A.硫酸和氯氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| B.碳酸钠与盐酸反应:Na2CO3+ 2H+=2Na+ +CO2↑+H2O |
| C.铁钉放入硫酸铁溶液中:Fe + Fe3+ = 2Fe2+ |
| D.Ca(NO3)2溶液和Na2CO3溶液混合:Ca2+ + CO32-=CaCO3↓ |
设NA为阿伏伽德罗常数的数值,下列叙述正确的是
A.已知N2(g)+3H2(g)  2NH3(g) △H=-92.4KJ/mol,在该反应中,当有3NA电子转移时,上述热化学反应方程式的焓变为△H=-46.2KJ/mol 2NH3(g) △H=-92.4KJ/mol,在该反应中,当有3NA电子转移时,上述热化学反应方程式的焓变为△H=-46.2KJ/mol |
| B.1L 0.1mol·L-1碳酸钠溶液的阴离子总数等于0.1NA |
| C.室温下pH=13的NaOH溶液中含有的OH-0.1NA |
| D.浓度分别为1mol·L-1和0.5mol·L-1的CH3COOH和CH3COONa混合液共1L,含CH3COOH和CH3COO-共1.5mol |
近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI+3H2O==KIO3+3H2↑。下列有关说法正确的是
| A.电解时,石墨作阴极,不锈钢作阳极 |
| B.电解时,阳极反应是:I--6e-+3H2O=IO-3+6H+ |
| C.溶液调节至强酸性,对生产有利 |
| D.电解过程中溶液的pH逐渐减小 |
下列说法正确的是
| A.工业用电解熔融AlCl3的方法制金属铝 |
| B.铅蓄电池工作时,正极反应为:PbO2+2e-+4H++SO42-=PbSO4+2H2O |
| C.电解饱和食盐水时,用铁作阳极,Cl-发生氧化反应 |
| D.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如右图所示。据图判断正确的是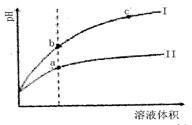
| A.II为盐酸稀释时的pH值变化曲线 |
| B.b点溶液的导电性比c点溶液的导电性强 |
| C.a点KW的数值比c点KW的数值大 |
| D.b点酸的总浓度大于a点酸的总浓度 |
下列过程或现象与水解无关的是
| A.纯碱溶液去油污 |
| B.配制氯化铁溶液时加入少量的盐酸 |
| C.NaHCO3与Al2(SO4)3混合作泡沫灭火剂 |
| D.铁在潮湿的环境下生锈 |