烃通过臭氧化并经锌和水处理得到醛或酮。
例如: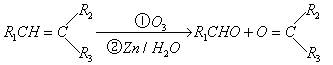
上述反应可用来推断烯烃的结构。一种链状单烯烃A通过臭氧化并经锌和水处理得到B和C。化合物B的相对分子质量是58,含碳62.1%,含氢10.3%,B无银镜反应,催化加氢生成D,D在浓硫酸存在下加热,可得到能使溴水褪色的物质E。反应图示如下: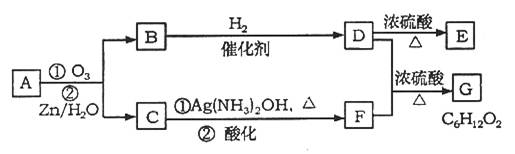
回答下列问题:
(1)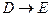 的反应类型为_____________;C中含有官能团的名称为___________;B的结构简式为 _________________。
的反应类型为_____________;C中含有官能团的名称为___________;B的结构简式为 _________________。
(2) 的化学方程式是__________________________________。
的化学方程式是__________________________________。
(3)A的结构简式为__________________________________________。
(4)化合物A的某种同分异构体通过臭氧化并经锌和水处理只得到一种产物,写出所有符合该条件的同分异构体的结构简式__________________、_____________。
(1)已知下列各反应的焓变
①Ca(s)+C(s,石墨)+3/2O2(g)=CaCO3(s)△H1 = -1206.8 kJ/mol
②Ca(s)+1/2O2(g)=CaO(s)△H2= -635.1 kJ/mol
③C(s,石墨)+O2(g)=CO2(g)△H3 = -393.5 kJ/mol
试求:④CaCO3(s)=CaO(s)+CO2(g)△H=________。
(2)已知下列各反应的焓变
①CO(g)+1/2O2(g)=CO2(g) ΔH1= -283.0 kJ/mol
②H2(g)+1/2O2(g)=H2O(l) ΔH2= -285.8 kJ/mol
③C2H5OH(l)+ 3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370 kJ/mol
试求:④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l) ΔH=________。
(8分)能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质。一定条件下,在体积为2 L的密闭容器中,1mol一氧化碳与2mol氢气反应生成甲醇(催化剂为Cu2O/ZnO):
CO(g)+2H2(g) CH3OH(g)△H<0
CH3OH(g)△H<0
根据题意完成下列各题:
反应达到平衡时,平衡常数表达式K=,升高温度,K值(填“增大”、“减小”或“不变”)。
(2)在500℃,10min反应达平衡,此时甲醇的物质的量浓度为0.3mol/L,从反应开始到平衡,氢气的平均反应速率v(H2)=。
(3)在其它条件不变的情况下,把反应处于平衡体系的容器的体积压缩为1 L,下列有关该体系的说法正确的是。
| A.平衡向正反应方向移动 | B.正反应速率加快,逆反应速率减慢 |
| C.甲醇的物质的量增加 | D.重新平衡时c(CO)/c(CH3OH)不变 |
(12分)(1)已知C(s、金刚石)+O2==CO2(g) ΔH=-395.4kJ/mol,
C(s、石墨)+O2==CO2(g) ΔH=-393.5kJ/mol。
①石墨和金刚石相比,石墨的稳定性金刚石的稳定性。
②石墨中C-C键键能______金刚石中C-C键键能。(均填“大于”、“小于”或“等于”)。
(2)肼(N2H4)和NO2是一种双组分火箭推进剂。两物质混合发生反应生成N2和H2O(g),已知8g气体肼在上述反应中放出142kJ热量,其热化学方程式为:。
(3)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为:;
又知H2O(l)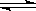 H2O(g),△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是kJ。
H2O(g),△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是kJ。
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)步骤②中的BaCl2溶液能否替换成以下溶液()
| A.Ba(NO3)2溶液 | B.Ba(OH)2溶液 |
| C.A和B均可以 | D.A和B均不可以 |
(2)第④步用到的试剂作用是;
(3)利用题干所给试剂,②③④所加试剂的顺序还可以是(填化学式);
(4)判断SO42-已除尽的方法是;
(5)若先用盐酸调溶液至酸性,再过滤,将对纯度产生影响,其可能的原因是(用相应的离子方程式表示),
(至少两个)。
27.2g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,ACl2的摩尔质量是,A的相对原子质量是。