(1)实验室里不同化学试剂的保存方法不尽相同,下图中A、B、C、D是常见的一些保存药品的试剂瓶,请把下列常见试剂的序号填写在各试剂瓶下面的括号内: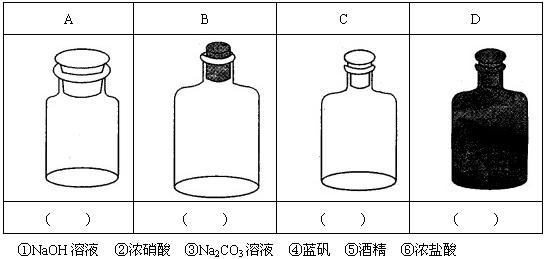
(2)用试纸检验NaOH溶液pH大小的操作方法是
根据物质的组成和性质将下列无机化合物进行了分类。
| 物质类别 |
酸 |
碱 |
盐 |
氧化物 |
氢化物 |
| 化学式 |
①H2SO4 ②______ |
③NaOH ④______ |
⑤Na2SO4 ⑥______ |
⑦SO2 ⑧Na2O |
⑨HCl ⑩_____ |
(1)请仔细观察表格中的物质类别,从K、H、O、C、N五种元素中任选两种或三种组成合适的物质,将化学式分别填在表中②、④、⑥、⑩后面的横线上。
(2)⑦和⑧可发生非氧化还原反应,生成一种盐。该反应的化学方程式为________________________________________________________________________。
(3)将⑦通入③的溶液中,反应的离子方程式为_______________________________________。
(4)⑨极易溶于水并电离出氯离子,大多数含氯离子的盐溶于水后也能电离出氯离子。检验溶液中氯离子的方法是_____________________________________________。
(1)现有以下物质:
aNaCl晶体;b液态SO3;c液态的醋酸;d汞;eBaSO4固体;f纯蔗糖;g酒精;h熔化的KNO3
请回答下列问题(填写相应的字母):
①以上物质中能导电的是________。
②以上物质中属于电解质的是____________。
③以上物质中属于非电解质的是____________。
④以上共价化合物中溶于水后形成的水溶液能导电的是______________。
(2)下列关于氧化物的各项叙述正确的是__________(填写序号)。
①酸性氧化物肯定是非金属氧化物 ②非金属氧化物肯定是酸性氧化物 ③碱性氧化物肯定是金属氧化物 ④金属氧化物都是碱性氧化物 ⑤酸性氧化物均可与水反应生成相应的酸 ⑥与水反应生成酸的氧化物不一定是酸酐,与水反应生成碱的氧化物不一定是碱性氧化物 ⑦不能跟酸反应的氧化物一定能跟碱反应
有机物A(C5H10O)能够发生如图所示的相关反应。已知A分子中含有2个位置不同的甲基,E属于烃类化合物。
(1)A的名称是,Ⅲ的反应类型是。
(2)试剂a最好是。
(3)A的一种同分异构体的核磁共振氢谱中有4个峰,该同分异构体的结构简式为。
(4)与B含有相同官能团的同分异构体有种。
(5)一定条件下,B与C反应生成有香味的有机化合物,写出该反应的化学方程式。
决定物质性质的重要因素是物质的结构。请回答下列问题:
(1)N、O、S三种元素的第一电离能从大到小的顺序为 。
(2)甲醛(H2C=O)分子碳原子的杂化方式为 用价层电子对互斥理论推断甲醛中H—C—H的键角120o(填“>”“<”或“=”)。
(3)科学家通过X射线探明,KCl、MgO、CaO的晶体结构与NaCl的晶体结构相似(图a所示)。KCl、CaO、MgO三种离子晶体熔点从高到低的顺序是。
(4)设MgO晶胞的边长为acm,则MgO的密度是g·cm-3(只要求列算式。阿伏加德罗常数为NA)。
(5)某配合物的分子结构如图b所示,其分子内不含有(填字母)。
| A.离子键 | B.共价键 | C.金属键 | D.配位键 E.氢键 F. 键 键 |

下图是某化学兴趣小组设计的利用电子垃圾(含70%Cu、25%Al、4%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线:
已知下列信息:
Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Cu(OH)2 |
| 开始沉淀 |
1.1 |
4.0 |
5.4 |
| 完全沉淀 |
3.2 |
5.2 |
6.7 |
请回答下列问题:
(1)写出Cu与稀硫酸和H2O2的混合液反应的化学方程式:.。
(2)在操作Ⅱ中,x的取值范围是。
(3)在操作Ⅲ中,蒸发浓缩需要的玻璃仪器有。
(4)由滤渣a制取Al2(SO4)3·l8H2O,探究小组设计了三种方案:
综合考虑上述三种方案,最具可行性的是(填序号)。
(5)为测定CuSO4·5H2O晶体的纯度,进行下列实验:取a g试样配成l00 mL溶液,每次取20.00mL,消除干扰离子后,用b mol·L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液l2.00 mL。(常温时,5%的Na2H2Y水溶液,其pH为4—6。)
①CuSO4·5H2O晶体的纯度是 。
②下列滴定方式中,最合理的是(夹持部分略去) (填序号)。