已知:①NaNO2具有强氧化性
②
奥沙拉秦是一种抗菌药。其合成路线如下:
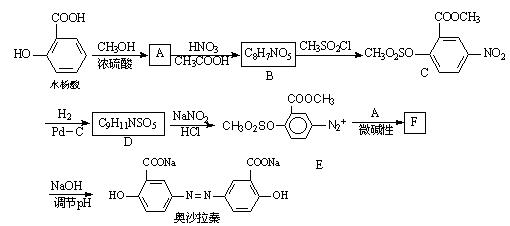
⑴写出下列反应的化学方程式:
水杨酸→A_____________________________________________;
A→B _________________________________________________。
⑵写出D的结构简式______________________。
⑶写出下列反应的反应类型:D→E______________,F→奥沙拉秦___________。
⑷整个合成路线看,设计B→C步骤的作用是___________________________。
⑸F的结构简式为___________________。
⑹有机物G(结构简式见下图)也可用于合成奥沙拉秦。它的一种同分异构体X是 -氨基酸,能与FeCl3发生显色反应,其分子中共有6种化学环境不同的H原子。X的结构简式为________________。
-氨基酸,能与FeCl3发生显色反应,其分子中共有6种化学环境不同的H原子。X的结构简式为________________。
有机物结构理论中,若一个碳原子同时含有两个羟基时,结构很不稳定,会自动脱水生成相应的醛: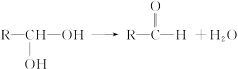
试写出甲烷与氯气光照后生成的一系列有机物中,在一定条件下与NaOH溶液共热后生成物的结构简式为:①____________,②____________,③____________,④____________。
已知:同一个碳原子上连有两个羟基时不稳定,会自动失水,即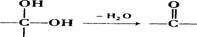
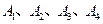 是化合物
是化合物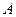 的四种同分异构体,它们的相对分子质量不超过l80.分子中只含碳、氢、氧三种元素,其中氧的质量分数为31.58%。实验表明:
的四种同分异构体,它们的相对分子质量不超过l80.分子中只含碳、氢、氧三种元素,其中氧的质量分数为31.58%。实验表明: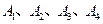 均是只有一个侧链的芳香族化合物,它们均含有醇羟基,并可以进行如下反应,产物中
均是只有一个侧链的芳香族化合物,它们均含有醇羟基,并可以进行如下反应,产物中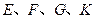 均为芳香族化合物。
均为芳香族化合物。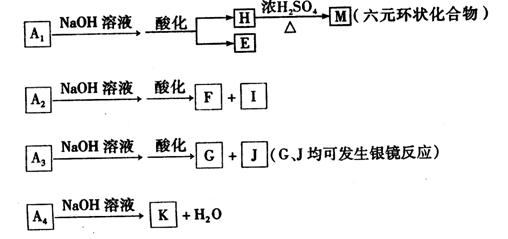
(1)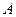 的相对分子质量为,分子式为。
的相对分子质量为,分子式为。
(2)写出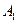 、
、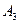 ,的结构简式。
,的结构简式。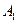 ;
;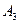 。
。
(3)写出由 生成
生成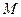 的化学反应方程式,反应类型为。
的化学反应方程式,反应类型为。
(4)现有如下试剂:稀盐酸、稀硫酸、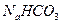 ,溶液和
,溶液和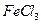 ,溶液。从中选择合适试剂,简述鉴别
,溶液。从中选择合适试剂,简述鉴别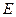 和
和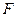 溶液的实验操作方法、现象及结论。
溶液的实验操作方法、现象及结论。
A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含一种官能团,且每个碳原子上最多只连一个官能团;A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请填空:
(1)A的分子式是_______________,其结构简式是___________________________________。
(2)写出A与乙酸反应的化学方程式:________________________________________。
(3)写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是______________________________________________________________________________。
碳正离子〔如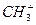 、
、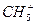 、(CH3)3C+等〕是有机反应中重要的中间体,欧拉(G.olah)因在此领域研究中的卓越成就而荣获1994年的诺贝尔化学奖。
、(CH3)3C+等〕是有机反应中重要的中间体,欧拉(G.olah)因在此领域研究中的卓越成就而荣获1994年的诺贝尔化学奖。
碳正离子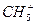 可以通过CH4在“超强酸”中再获得一个H+而得到,而
可以通过CH4在“超强酸”中再获得一个H+而得到,而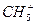 失去H2可得
失去H2可得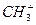 。
。
(1)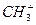 是反应性很强的正离子,是缺电子的,其电子式是_____________。
是反应性很强的正离子,是缺电子的,其电子式是_____________。
(2)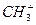 中4个原子是共平面的,三个键角相等,键角应是_____________(填角度)。
中4个原子是共平面的,三个键角相等,键角应是_____________(填角度)。
(3)(CH3)2CH+在NaOH的水溶液中反应将得到电中性的有机分子,其结构简式是________。
(4)(CH3)3C+去掉H+后将生成电中性的有机分子,其结构简式是_____________。
某饱和一元醇的分子式为CnH2n+2O。
(1)若该醇没有同分异构体,则该醇的结构简式为:______________________________。
(2)若该醇有同分异构体,且各同分异构体分别跟浓H2SO4加热发生消去反应生成同一种烯烃,则该醇的分子式为:_____________________________,其同分异构体的结构简式分别为:__________________________________________。