下列说法正确的是( )
| A.第ⅥIA族元素从上到下,其氢化物的还原性依次减弱 |
| B.同周期从左到右,非金属元素最高价氧化物对应的水化物的酸性依次增强 |
| C.第三周期元素的离子半径从左到右逐渐减小 |
| D.CCl4属于共价化合物,每个原子都满足8电子结构,其水溶液能导电 |
向一定体积的0.1摩/升的醋酸溶液中加入等体积的蒸馏水后,则下列叙述正确的是
| A.溶液的pH值变小 |
| B.醋酸的电离度增大 |
| C.溶液的导电能力减弱 |
| D.中和此溶液所需的0.1摩/升NaOH溶液的体积增加 |
在373K时,N2O4  2NO2 △H>0把0.5molN2O4气体通入体积为5L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法不正确的是
2NO2 △H>0把0.5molN2O4气体通入体积为5L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法不正确的是
| A.前2s,N2O4的平均反应速率为0.005mol·L-1·s-1 |
| B.平衡时,N2O4的转化率为50% |
| C.平衡时,体系内NO2为0.04mol·L-1 |
| D.在2s时,体系内压强为反应前的1.1倍 |
在一定温度下的定容密闭容器中,当物质的下列物理量不再发生变化时,表明反应A(g)+2B(g) C(g)+D(g)已达到平衡状态的是
C(g)+D(g)已达到平衡状态的是
| A.混合气体的密度 | B.混合气体的总物质的量 |
| C.混合气体的压强 | D.混合气体的总体积 |
右图是关于反应A2(g)+3B2(g) 2C(g) ⊿H<的平衡移动图象,影响平衡移动的原因可能是
2C(g) ⊿H<的平衡移动图象,影响平衡移动的原因可能是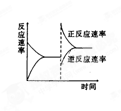
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
通常人们把拆开1 mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
| 化学键 |
A—A |
B—B |
A—B |
| 生成1 mol化学键时放出的能量 |
436 kJ·mol-1 |
243 kJ·mol-1 |
431 kJ·mol-1 |
则下列热化学方程式不正确的是()
A.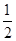 A2(g)+
A2(g)+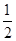 B2(g)=AB(g)ΔH=-91.5 kJ·mol -1
B2(g)=AB(g)ΔH=-91.5 kJ·mol -1
B.A2(g)+B2(g)=2AB(g)ΔH=-183 kJ·mol -1
C.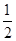 A2(g)+
A2(g)+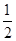 B2=AB(g)ΔH=+91.5 kJ·mol-1
B2=AB(g)ΔH=+91.5 kJ·mol-1
D.2AB(g)=A2(g)+B2(g)ΔH=+183 kJ·mol-1