反应C(s)十H2O(g) 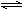 CO(g)十H2(g) 在一密闭容器中进行,下列条件的改变能使反应速率减小的是
CO(g)十H2(g) 在一密闭容器中进行,下列条件的改变能使反应速率减小的是
| A.减少C的量 | B.容积不变,增加水蒸气的量 |
| C.升温 | D.压强不变,充入Ne |
下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是()
X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若用惰性电极电解Y2+和Z2+共存的溶液时,Y先析出;又知M+X2+  M2++X。则这四种金属的活动性由强到弱的顺序为
M2++X。则这四种金属的活动性由强到弱的顺序为 ()
()
| A.X>Z>Y>M | B.M >X> Z > Y | C.M>Z>X>Y | D.X>Z>M>Y |
某醇与足量的金属钠反应,产生的氢气与醇的物质的量之比为1∶1,则该醇可能是()
| A.甲醇 | B.乙醇 | C.乙二醇 | D.丙三醇 |
下列对分子结构叙述不正确的是()
| A.H2O2分子中,两个O之间形成1对共用电子对 | B.N2的电子式是N┇┇N |
| C.CCl4和甲烷都是正四面体型分子 | D.CO2和CS2都是直线型分子 |
下列不能用勒夏特列原理解释的是()
| A.Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| B.棕红色NO2加压后颜色先变深后变浅 |
| C.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D.合成氨工业中通入过量氮气可提高H2转化率 |