已知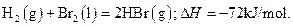 蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
| |
H2(g) |
Br2(g) |
HBe(g) |
| 1mol分子中的化学键断裂需要吸收的热量/kJ |
436 |
a |
369 |
则表中a为
| A.404 | B.260 | C.230 | D.200 |
下列说法正确的是
A.标况下22.4 L/mol就是气体摩尔体积 L/mol就是气体摩尔体积 |
| B.非标况下,1mol任何气体的体积不可能为22.4L |
| C.标况下22.4L任何气体都含有约6.02x1023个分子 |
| D.1molH2和O2混合气体在标况下的体积为22.4L/mol |
若用NA表示阿伏加德罗常数的值,则下列说法错误的是
| A.常温常压下22.4 LH2含2NA个电子 | B.NA个O2和NA个H2的质量比为16 : 1 |
| C.1molH2O总共含有3NA个原子 | D.71g Cl2变为Cl--可得到2NA个电子 |
如果你家里的食用花生油混有水份,你将采用下列何种方法分离
| A.过滤 | B.蒸馏 | C.分液 | D.萃取 |
在20g密度为dg/cm3的硝酸钙溶液里含1g Ca2+,则NO3-离子的物质的量浓度是
A.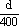 mol·L-1 mol·L-1 |
B. mol·L-1 mol·L-1 |
C.2.5d mol·L-1 | D.1.25 d mol·L-1 |
在0.5L某浓度的 NaCl 溶液中含有0.5mol Na+,对该溶液的说法不正确的是
| A.该溶液的物质的量浓度为 1 mol·L-1 |
| B.该溶液中含有58.5g NaCl |
| C.配制100 mL该溶液需用5.85g NaCl |
| D.量取100 mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1 mol |