下列分子或离子中的中心原子杂化轨道的类型不相同的是  ( )
( )
| A.NO3-、CH2O | B.NH3、SO42- | C.苯和乙烯 | D.CO2、SO2 |
 下列各组物质中,化学键类型完全相同的是
下列各组物质中,化学键类型完全相同的是
| A.N2和NaOH | B.CO2和H2O | C.MgO和NaCl | D.HCl和KCl |
下列各组物质的性质依次递减的是
| A.碱性:Al(OH)3、Mg(OH)2、NaOH | B.还原性:HI、HBr、HCl |
| C.酸性:HClO4、H2SO4、H3PO4 | D.稳定性:H2CO3、NaHCO3、Na2CO3 |
可逆反应N2+3H2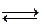 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
| A.3v正(N2)=v正(H2) | B.2v正(N2)=v逆(NH3) |
| C.v正(N2)=3v逆(H2) | D.2v正(H2)=3v逆(NH3) |
哈伯因发明用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在一定条件下使该反应发生。下列说法正确的是


A.达到化学平衡时,N2完全转化为NH3 |
B.一定条件下达到化学平衡后,反应体系中的压强保持不变 |
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 |
D.达到化学平衡时,正反应和逆反应速率都为零 |
用铜、银和硝酸银溶液设计一个原电池,下列对该原电池的判断正确的是
| A.铜作负极被氧化 | B.银为正极被还原 |
| C.正极反应为:Ag+ + e-="Ag" | D.NO3-向正极移动 |