设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A.标准状况下,1 LH2O所含分子数为1/22.4NA |
| B.常温常压下,11.2 LCO2所含的分子数为0.5NA |
| C.常温常压下,32 g O2含有的氧原子数为2NA |
| D.标准状况下,22.4 L H2中所含原子数为NA |
氨水中所含有的分子和离子有()
①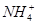 ②H2O③NH3④NH3·H2O⑤H+⑥OH-
②H2O③NH3④NH3·H2O⑤H+⑥OH-
| A.①②③ | B.②③④⑤ | C.②③④⑤⑥ | D.①②③④⑤⑥ |
下图是一种航天器能量储存系统原理示意图.下列说法正确的是( )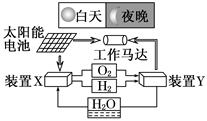
| A.该系统中只存在三种形式的能量转化 |
| B.装置Y中负极的电极反应式为:O2+2H2O+4e-===4OH- |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
银器的保护主要是维持它的原貌,对于轻微腐蚀蒙有硫化银的银器,可将其和铝片一起接触浸泡在稀NaOH溶液中,经一定时间污迹消失,取出后用水洗于净,再用软布或棉团擦光。有关叙述不正确的是()
| A.溶液中的OH-离子向负极移动 |
| B.在银表面上的反应为:Ag2S+2e-=2Ag+S2- |
| C.在铝表面的反应为:Al-3e-=Al3+ |
| D.在铝表面的反应为:Al+4OH-+3e-=AlO2-+2H2O |
下列各组中的X和Y两种原子,在周期表中一定位于同一族的是( )
| A.X原子和Y原子最外层都只有一个电子 |
| B.X原子的核外电子排布为1s2,Y原子的核外电子排布为1s22s2 |
| C.X原子2p能级上有三个电子,Y原子的3p能级上有三个电子 |
| D.X原子核外M层上仅有两个电子,Y原子核外N层上也仅有两个电子 |
用惰性电极电解饱和Na2CO3溶液,若保持温度不变,则一段时间后()
| A.溶液的pH变大 | B.c(Na+)与c (CO32-)的比值变大 |
| C.溶液浓度变大,有晶体析出 | D.溶液浓度不变,有晶体析出 |