设NA为阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,46gNO2和N2O4混合气体中含有的分子数为NA |
| B.标况下,2.24L的H2O所含氢原子数大于0.2NA |
| C.常温下1L0.1 mol/L醋酸溶液中,水电离的氢离子数为10—13NA |
| D.水蒸气通过足量Na2O2使其增重ag时,转移的电子数为aNA |
下列各组离子在指定溶液中一定能大量共存的是
①无色溶液中:K+、Na+、NO3—、Cr2O72—
②pH=1的溶液中:C2O42-、Na+、S2O32-、SO42-
③水电离的c(H+)=1×10-13 mol•L—1的溶液中: Fe2+、NO3—、S2—、AlO2—
④加入Mg粉能放出H2的溶液中:Mg2+、NH4+、K+、Cl—
⑤碱性溶液中:K+、 Na+、NO3-、I—
| A.④⑤ | B.③⑤ | C.②④ | D.①② |
在恒容密闭容器中,CO与H2发生反应CO(g)+2H2(g) 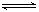 CH3OH(g)达到平衡后,若只改变某一条件,下列示意图正确的是
CH3OH(g)达到平衡后,若只改变某一条件,下列示意图正确的是
将标准状况下2.24L CO2缓慢通入1L 0.15 mol•L—1的NaOH溶液中,气体被充分吸收,下列关系不正确的是
| A.c(Na+)+c(H+)=c(OH—)+c(HCO3—)+2c(CO32—) |
| B.2c(Na+)=3[c(H2CO3)+c(HCO3—)+c(CO32—)] |
| C.c(Na+) > c(CO32—) > c(HCO3—)> c(OH—)> c(H+) |
| D.2c(OH—)+ c(CO32—)= c(HCO3—)+ 3c(H2CO3)+2c(H+) |
下列说法正确的是
| A.向等体积的20%的H2O2溶液和10%的H2O2溶液中分别滴加等体积的0.1mol•L—1 FeCl3溶液和0.1 mol•L—1CuCl2溶液,前者产生气泡快,这个实验可以充分证明催化剂具有选择性 |
| B.利用水解反应可以制取某些无机化合物如TiO2、SnO2等 |
| C.将0.1 mol•L—1醋酸加水稀释,溶液中各离子浓度均减小 |
| D.室温下同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |