在化学上,常用短线表示化学键。在如图所示的结构中,直线不表示化学键或不完全表示化学键的是( )
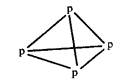
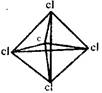

| A.石墨 | B.白磷 | C.CCl4 | D.C8H8(立方烷) |
下列变化,加入氧化剂才能实现的是
| A.Na2S→H2S | B.CO2→CO | C.FeO→Fe2O3 | D.AlCl3→Al(OH)3 |
下列有关二氧化硅的叙述中不正确的是
| A.沙子、石英、水晶的主要成分都是SiO2 |
| B.SiO2是制光导纤维的主要原料 |
| C.硅酸可由SiO2直接制得 |
| D.SiO2是酸性氧化物,一定条件下可与碱性氧化物或碱反应 |
将一小块钠投入盛20 mL饱和澄清石灰水的烧杯里,不可能观察到的现象应是
| A.钠熔成小球、四处游动 | B.钠浮在液面上 |
| C.溶液底部有银白色物质生成 | D.溶液变浑浊 |
医生建议患甲状腺肿的病人多食海带,这是由于海带中含较丰富的
| A.碘元素 | B.铁元素 | C.钾元素 | D.锌元素 |
下列物质中不属于硅酸盐的是
| A.陶瓷 | B.玻璃 | C.水晶 | D.水泥 |