苯佐卡因是一种局部麻醉剂,可用于粘膜溃疡、创面及痔疮的镇痛,一般制成软膏或栓剂合用。其合成路线如下图所示,其中有机物B具有酸性。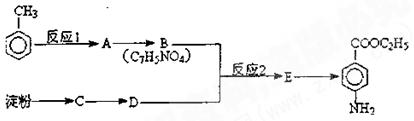
已知:①苯环上的取代反应有如下定位规律:当苯环上的碳原子连有甲基时,可在其邻位或对位上引入官能团;当苯环上的碳原子连有羧基时,可在其间位上引入官能团;
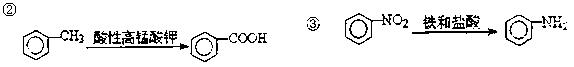
(1)反应类型:反应1 ;反应2 ;
(2)化合物A、C的结构简式:A ;C ;
(3)写出下列转化的化学方程式
C→D:
B+D→E:
(4)苯莽卡因有多种同分异构体,其中氨基直接连在苯环上,分子结构中含有-COOR官能团,且苯环上的一氯代物只有两种的同分异构体共有六种,除苯佐卡因外,其中三种的结构简式为: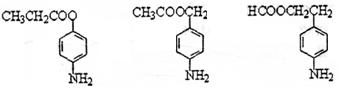
则剩余两种同分异构体的结构简式为: 、 。
在63Li、73Li、2311Na、2412Mg、146C、147N中
(1)63Li和73Li 互称,它们的化学性质;
(2)146C和147N的相等,2311Na和2412Mg的相等;
(3)2412Mg的电子所占据的电子层中,能量最高的是层(填符号)。
某有机物10.8g完全燃烧生成7.2g水和15.68L(标准状况)二氧化碳,0.25mol此有机物质量为27g
(1)此有机物的分子式为。
(2)又知此有机物有弱酸性,能与金属钠反应,也能与氢氧化钠溶液反应,试推断此有机物的结构,写出可能的结构简式。
快乐是什么?精神病学专家通过实验发现:在大脑的相应部位—“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺结构如右图: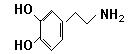
(1)多巴胺分子式: 。
(2)试判断多巴胺能发生的化学反应()
| A.加成 | B.取代 | C.氧化 | D.水解 |
(3)写出与多巴胺互为同分异构体且符合下列条件的物质的结构简式:
(a)属于1、3、5三取代苯(b)苯环上直接连有一个羟基和一个氨基
(c)分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2︰1。
、 。
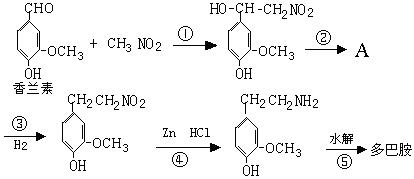
(4)多巴胺可由香兰素与硝基甲烷缩合,再经锌汞齐还原水解而得。合成过程表示如下:
|
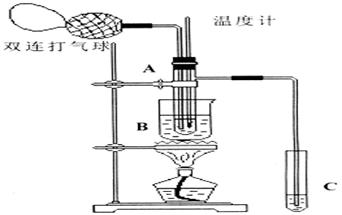
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有 某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
| 物质 |
乙醛 |
乙酸 |
甘油 |
乙二醇 |
水 |
| 沸点 |
20. 8℃ 8℃ |
117.9℃ |
290℃ |
197.2℃ |
100℃ |
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)____________________________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在_____________;目的是____________________;当试管A内的主要反应完成后温度计水银球的位置应在____________,目的是_______________________;
(3)烧杯B的作用是_ __________________________;烧杯B内盛装的液体可以是____________(写出一种即可,在题给物质中找);
__________________________;烧杯B内盛装的液体可以是____________(写出一种即可,在题给物质中找);
质谱图表明某有机物的相对分子质量为70,红外光谱表征到C==C和C==O的存在, 核磁共振谱如下图(峰面积之比依次为1:1:1:3);分析核磁共振谱图,回答下列问题:
核磁共振谱如下图(峰面积之比依次为1:1:1:3);分析核磁共振谱图,回答下列问题:
(1)分子中共有种化学环境不同的氛原子。
(2)该物质的分子式为
(3)该有机物的结构简式为。