有Fe和Fe2O3的混合物溶于500ml的稀硝酸中,放出NO22.4L(标况下)并余5.44g Fe,向反应后的溶液中通入20.16LCl2(标况),恰好能使溶液中的Fe2+全部氧化。求:(1)稀硝酸的物质的量浓度 (2)混合物中Fe的质量分数
臭氧能与KI溶液反应,生成一种可使带余烬的木条复燃的气体,向反应后溶液中滴入酚酞变成红色,若滴入淀粉溶液则变成蓝色。为测定大气中臭氧的含量,将0℃,1.01×105Pa,33.6m3的空气通过KI溶液,使之完全反应,在所得溶液中用0.01mol/L的Na2S2O3溶液60mL恰好与之反应完全(反应式为</PGN0047A.TXT/PGN>2Na2S2O3+I2=Na2S4O6+2NaI)。
(1)完成下列方程式:O3+KI+H2O→____
(2)计算大气中臭氧的体积分数。
吗啡是严格查禁的毒品。吗啡分子含C 71.58%、H 6.67%、N 4.91%、其余为O。已知其分子量不超过300。试求:(1)吗啡的分子量;(2)吗啡的分子式。
(1)吗啡的分子量是____,分子式是____。
(2)海洛因的分子量是____,分子式是____。
将n mol木炭粉和1 mol氧化亚铁在反应器中混合,隔绝空气加强热。
(1)可能发生的化学反应有:
①FeO+C=Fe+CO↑②2FeO+C=2Fe+CO2↑
③FeO+CO=Fe+CO2↑④____
物是____。
(3)若n>4,充分反应后,反应器中的固体物质是,____气体产物是____。
(4)若反应的气体产物是混合物,n的取值范围是____。
(5)若反应的气体产物是混合物,且混合物中CO和CO2的物质的量相等,则n的值为____。
标准状况下,a L Cl2通入到1 Lb mol/L的FeI2溶液中,充分反应后,所得溶液中Fe2+的物质的量浓度与a、b的关系如下表,请完成其余空格。
| a、b的关系 |
Fe2+的物质的量浓度(mol/L) |
| a≤22.4b |
①___ |
| ②_____ |
0 |
| 22.4b≤a≤33.6b |
③____ |
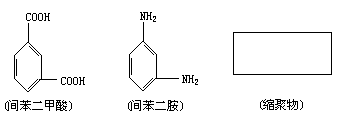
Nomex纤维是一种新型阻燃纤维。它可由间苯二甲酸和间苯二胺在一定条件下以等物质的量的缩聚而成的。请把Nomex纤维结构简式写在下面的方框中。