下列说法正确的是
| A.常温下若强酸、强碱等体积中和后pH=7,则中和之前pH酸+pH碱=14 |
| B.为绘制中和滴定曲线,在滴定过程中,每隔相同时间用pH计测定一次锥形瓶中溶液的pH |
| C.测定溶液的pH时,应先将pH试纸润湿,然后进行检测 |
| D.在pH=12的溶液中,水电离出的c(OH-)=10-2mol·L-1 |
下列化学用语表示正确的是
| A.铁原子的电子排布式:[Ar]3d64s2 | B.核内有8个中子的碳原子: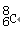 |
C.氢氧化钠的电子式: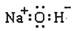 |
D.F的原子结构示意图: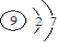 |
下列事实不属于盐类水解应用的是( )
| A.明矾、氯化铁晶体常用于净水 | B.实验室制氢气时加CuSO4可加快反应速率 |
| C.实验室配制FeCl3溶液时加入少量稀盐酸 | D.实验室通常使用热的纯碱溶液去除油污 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+H2O(g)  CO2+H2(g),反应过程中测定的部分数据见下表(表中t1>t2):
CO2+H2(g),反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min |
n(CO)/mol |
H2O/ mol |
| 0 |
1.20 |
0.60 |
| t1 |
0.80 |
|
| t2 |
0.20 |
下列说法正确的是
A.反应在t1min内的平均速率为
B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时n(CO2)=0.40 mol。
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
下列溶液中各微粒的浓度关系不正确的是
| A.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4的溶液中,c(NH4+)大小:①=②>③ |
| B.常温下,在10mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL |
| C.25℃时,浓度均为0.1 mol·L-1的NH3·H2O、NH4Cl溶液等体积混合,所得溶液显碱性:c(NH4+)+c(H+)>c(NH3·H2O)+c(OH-) |
| D.浓度均为0.1mol/L的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-) |
下列说法正确的是
| A.将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为氢氧化钠 |
| B.向FeI2溶液中通入少量Cl2,再滴加少量CCl4,振汤、静置,下层液体为紫色 |
| C.将SO2气体通入溴水,欲检验是否有SO42-生成,可向溶液中滴加Ba(NO3)2溶液 |
D.一定温度下,反应MgCl2(1) ="=Mg(1)+" Cl2(g)的 |