下列事实不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+H2O HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅。 HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅。 |
B.对CO(g)+NO2(g) CO2(g)+NO(g),平衡体系增大压强可使颜色变深。 CO2(g)+NO(g),平衡体系增大压强可使颜色变深。 |
| C.升高温度能够促进水的电离。 |
| D.工业上合成NH3的反应,为提高NH3的产率,理论上应采取相对较低温度的措施。 |
据2006年11月12日中央电视台每周质量报道,北京市场上销售的一部分标称是白洋淀特产的“红心鸭蛋”含偶氮染料“苏丹红Ⅳ号”,国际癌症研究机构将其列为三类致癌物。“苏丹红Ⅳ号”的结构简式: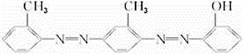 ,
,
下列关于“苏丹红Ⅳ号”说法正确的是( )
| A.属于芳香烃 | B.属于甲苯同系物 |
| C.化学性质跟苯完全相同 | D.能发生加成反应 |
下列关于有机物描述不正确的是()
| A.绝大多数有机物易溶于有机溶剂,难溶于水 |
| B.所有机物均可以燃烧,多数都是非电解质 |
| C.有机物所参与的反应一般比较复杂,所以用箭头连接 |
| D.甲烷是最简单的有机化合物 |
一定条件下,可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol· L-1、0.3mol· L-1、0.08mol· L-1,则下列判断不正确的是()
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol· L-1、0.3mol· L-1、0.08mol· L-1,则下列判断不正确的是()
| A.c1:c2的值不能确定 | B.平衡时,Y和Z的生成速率之比为3:2 |
| C.0.28mol·L-1<c1+c2+c3< 0.56mol·L-1 | D.c1的取值范围为0<c1<0.14 mol·L-1 |
可以证明乙醇分子中有一个氢原子与另外氢原子不同的方法是()
| A.1mol乙醇完全燃烧生成3mol水 | B.乙醇催化氧化变乙醛 |
| C.乙醇可以制饮料 | D.1mol乙醇跟足量的Na作用得0.5molH2 |
将0.5mol丙烷完全燃烧后生成的气体全部缓慢通入1L 2mol/LNaOH溶液中,生成的 Na2CO3和NaHCO3的物质的量之比为()
| A.3:2 | B.2:3 | C.2:1 | D.1:2 |