化学反应的实质是旧键的断裂和新键的形成过程,下列变化中不属于化学变化的是( )
| A.白磷在260℃转化为红磷 | B.石墨在高温高压下转化为金刚石 |
| C.干冰转化为CO2气体 | D.固态S8加热到444.6℃转化为硫蒸气S2 |
茉莉醛具有浓郁的茉莉花香,其结构简式如下图所示: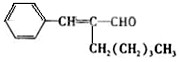
关于茉莉醛的下列叙述错误的是:
| A.能被高锰酸钾酸性溶液氧化 |
B.在加热和催化剂作用 下,能被氢气 下,能被氢气 还原,且1mol最多可耗H2 5mol 还原,且1mol最多可耗H2 5mol |
C.在一定 条件下能与Br2(g)发生取代反应 条件下能与Br2(g)发生取代反应 |
| D.不能HBr发生加成反应 |
A、B两种有机物组成的混合物,当其质量相等时,无论A、B以何种比例混合,完全燃烧时产生H2O的量均相等,符合这一条件的组合是
①同分异构体②同系物③最简式相同④含氢质量分数相同
⑤分子中氢原子数相同⑥分子中氢、氧原子数分别相同
A.①②③ B.①③④ C.①⑤⑥ D.②④⑥
工业上将苯的蒸气通过赤热的铁合成一种可作传热载体的化合物,该化合物分子中苯环上的一氯代物有3种,1mol该化合物催化加氢时最多消耗6mol氢气,判断这种化合物可能是
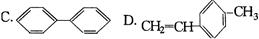
将 转变为
转变为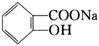 的方法是
的方法是
| A.与足量NaOH溶液共热,再通入足量CO2气体 |
| B.与稀硫酸共热后,再加入足量NaOH溶液 |
| C.加热该物质的溶液,再通入足量的Na |
| D.与稀硫酸共热后,加入足量的Na2CO3溶液 |
如图表示4—溴环己烯所发生的4个不同反应。其中,产物只含有一种官能团的反应是
| A.①④ | B.③④ | C.②③ | D.①② |