乙醇催化氧化为乙醛过程中化学键的断裂与形成情况可表示如下: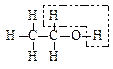

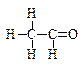 (注:含-CHO的物质为醛类化合物)
(注:含-CHO的物质为醛类化合物)
下列醇不能被氧化为醛类化合物的是()
| A.CH3OH | B.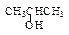 |
C.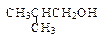 |
D.CH3CH2CH2OH |
下列比较关系与排列顺序不正确 的是()
的是()
| A.酸性:H4SiO4<H3PO4<H2SO4<HClO4 |
| B.熔沸点:HF<HCl<HBr<HI |
| C.还原性:SiH4>NH3>H2O>HF |
D.半径:Al3 +<Mg2+<Na+<F- +<Mg2+<Na+<F- |
NA代表阿伏加德罗常数。下列有关叙述正确的是()
| A.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2 NA个电子 |
| B.标准状况下,2.24L H2O含有的分子数等于0.1NA |
| C.24g镁原子最外层电子数为NA |
| D.3.4g NH3中含N—H键数目为0.2NA |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是()
A .原子半径 A>B>D>C
.原子半径 A>B>D>C
B.原子序数 d>c>b>a
C.离子半径 C3->D->B+>A2+
D.单质的还原性 A>B>D>C
50mL三种气态烃以任意比混合与足量的氧气混合点燃爆炸后,恢复到原来状态(常温常压)体积缩小100mL,则三种烃是()
| A.C2H6、C3H6、C4H6 |
| B.CH4、C2H4、C3H4 |
| C.C2H4、C3H6、C2H2 |
| D.CH4、C2H6、C3H8 |