氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答: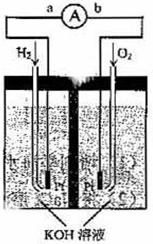
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b表示)。
(2)负极反应式为 。
(3)电极表面镀铂粉的原因为
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2 2LIH
2LIH
Ⅱ.LiH+H2O==LiOH+H2↑
反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下: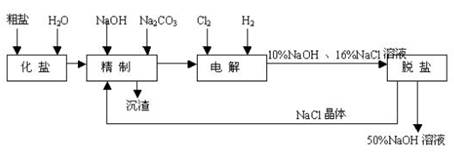
依据上图,完成下列填空:
(1)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为
,
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是
(选填a、b、c,多选扣分)
A. Ba(OH)2 B. Ba(NO3)2 C. BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
(选填a,b,c多选扣分)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3
(4)电解过程的总反应方程为。
(5)电解槽阳极产物可用于
(至少写出两种用途)。
80℃时,将0.40mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 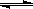 2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) |
0 |
20 |
40 |
60 |
80 |
100 |
| n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
| N(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)计算20s—40s内用N2O4表示的平均反应速率为mol·L-1·s-1
(2)计算在80℃时该反应的平衡常数K=;
(3)要增大该反应的K值,可采取的措施有(填序号);
| A.增大N2O4的起始浓度 | B.向混合气体中通入NO2 |
C.使用高效催化剂 | D.升高温度 |
(4)如右图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。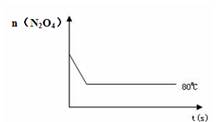
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁
年产量的1/4。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式。
正极:;负极:。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用下图所示甲的方案,其中焊接在铁闸门的固体材料R可以采用。(请写出具体金属名称)
(3)下图中乙方案也可降低铁闸门腐蚀速率,其中铁闸门应该连接在直流电源
的极。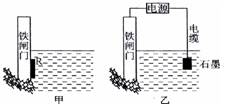
将镁、铝的混合物0.1mol 溶于100mL 2mol/LH2SO4溶液中,然后在得到的溶液中滴加1mol/LNaOH 溶液,请回答:
(1)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好完全沉淀,则加入NaOH溶液的体积是V(NaOH)=________mL。
(2)若在滴加NaOH溶液过程中,沉淀的质量随加入NaOH溶液的体积变化如下图所示。当V1=160mL时,求金属粉末中镁的物质的量和V2的体积?(要求写出解题过程)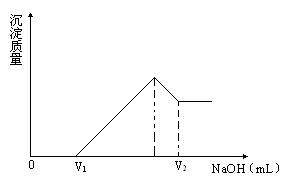
(3)若混合物仍为0.1mol ,其中Mg的物质的量分数为a,用100mL 2mol/L的H2SO4溶解此混合物后,再加入450mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3,则满足此条件的a的取值范围为。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
① 写出制取高铁酸钠的化学方程式:;
② 在制取高铁酸钠的反应中元素被氧化;
③ 高铁酸钠杀菌作用是利用了其具有的,而净水作用的原因是。
(2)在某化工厂生产中,要用到一种无色、可溶于水的晶体铝铵矾。该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵。向该复盐的溶液中逐滴加入氢氧化钠溶液,将发生一系列变化。已知,NH4+与AlO2-在水溶液中不能大量共存,会发生如下反应:NH4++A1O2-+H2O=Al(OH)3↓+ NH3↑ ,试回答:
① 硫酸铝铵在水溶液中的电离方程式为;
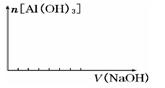
②在向该复盐的溶液中逐滴加入氢氧化钠溶液,请在下图中画出加入氢氧化钠溶液的体积与沉淀物质的量之间的关系。