下列说法正确的是( )。
| A.含有H+离子的溶液一定呈酸性 |
| B.0.1 mol/L KOH溶液和0.1 mol/L氨水中,其c(OH-)相等 |
| C.pH为1的盐酸的c(H+)是pH为3的盐酸的100倍 |
| D.Na2 CO3溶液中,c(Na+)是c(CO32-)的两倍 |
下列叙述正确的是( )
| A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42- |
| B.常温时,0.1mol/LHA溶液的pH>1,0.1mol/LBOH溶液中c(OH-)/c(H+)=1012,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为: c(B+)>c(OH-)>c(H+)>c(A-) |
| C.过量SO2通入到Ba(NO3)2溶液中,正确的离子反应方程式为: 3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+ |
D.用pH=3和p H=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va>10Vb H=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va>10Vb |
如图为某有机物的结构简式。已知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢化过程中不变,其反应原理如下:在铜铬氧化物催化下,R1COOR2+2H2→R1CH2OH+R2OH关于该化合物的下列说法中,正确的是( )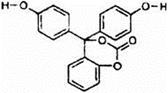
| A.该有机物的化学式为C20H14O5,该有机物可以属于酯类、酚类、醚类 |
| B.该有机物可以与浓溴水发生加成反应 |
| C.与足量氢氧化钠溶液充分反应,1mol该有机物最多可以与5molNaOH反应,所得产物中有醇类物质 |
| D.1mol该有机物在铜铬氧化物催化下仅能与2mol氢气发生反应 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B.常温下,46g分子式为C2H6O的物质中一定含有极性键为7NA,非极性键为NA |
| C.125mL16mol/L浓硫酸与足量的铜反应,生成SO2的分子数小于NA |
| D.标准状况下,体积为22.4LNO2、N2O4的混合气体,升温至常温,则混合气体分子数为NA |
下列各项内容中,排列顺序正确的是( )
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②相同pH的下列溶液中NH4+的浓度:(NH4)2SO4>NH4Cl>NH4HSO4
③氢化物的沸点:H2Se>H2S>H2O
④给出质子的能力:CH3COOH>NaHCO3> Al(OH)3
Al(OH)3
| A.①③ | B.①④ | C.①② | D.③④ |
常温下,将CH3COOH和KOH溶液混合,所得溶液PH=7,则此溶液中有()。
A c(CH3COO-)>c(Na+)
B c(CH3COO-)<c(Na+)
C c(CH3COO-)=c(Na+)
D 无法确定c(CH3COO-)与c(Na+)的关系