 C-NMR(核磁共振)可以用于含碳化合物的结构分析,有关
C-NMR(核磁共振)可以用于含碳化合物的结构分析,有关 C的说法正确的是
C的说法正确的是
| A.质子数为6 | B.电子数为13 | C.中子数为6 | D.质量数为6 |
自来水可以用氯气消毒。如果实验室中临时没有蒸馏水,可以用自来水配制某些急需的药品,但有些药品若用自来水配制,则明显会导致药品变质。下列哪些药品不能用自来水配制
| A.Na2SO4 | B.NaCl | C.AgNO3 | D.AlCl3 |
将4.6 g金属钠投入到95.6 g的水中,得到的溶液溶质的质量分数是
| A.4.6% | B.7.6% | C.8% | D.10% |
制取氯气时,下列尾气吸收方法最合理的是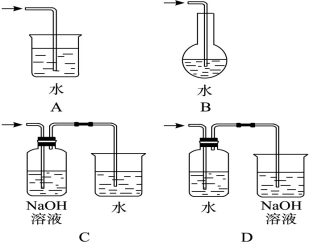
10 g 10%的氢氧化钠溶液稀释成50 mL,所得氢氧化钠溶液的物质的量浓度为
A、0.02 mol/L B、0.05 mol/L
C、0.25 mol/L D、0.5 mol/L
2.16g X2O5中含有0.1mol O,则X的相对原子质量为
| A.16 | B.28 | C.14 | D.31 |