将羧酸的碱金属盐电解可得到烃类化合物。例如:
2CH3COOK+2H2O CH3-CH3+2CO2↑+H2↑+2KOH
CH3-CH3+2CO2↑+H2↑+2KOH
请根据下列表示的衍变关系,回答问题。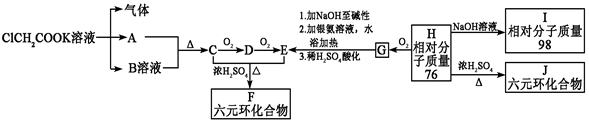
(1)写出下列物质的结构简式A: E: I
(2)G能发生反应的类型有(填序号):
a.取代 b.加成 c.还原 d.氧化 e.消去 f.水解
(3)写出H的最简单的两种同系物的结构简式 , 。
(4)F与J的关系为 (填序号) a.同一物质 b.同系物 c.同分异构体 d.同素异形体
(5)写出下列过程的化学方程式:
C→D: C+E→F:
某烃能使KMnO4溶液褪色,但不能使溴水褪色,其分子式为C8H10,该烃的一氯代物有三种(含侧链取代物),该烃的结构简式是_____________;若C8H10分子中苯环上的一氯代物有三种,则其结构简式为_______或________。
下列物质中互为同系物的有,互为同分异构体的有,
互为同素异形体的有 ,属于同位素的有, 是同一种物质的有。
⑴液氯
⑵ 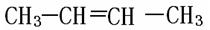
⑶白磷⑷氯气⑸氯水
⑹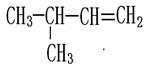 ⑺红磷⑻3717Cl
⑺红磷⑻3717Cl
⑼ 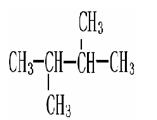
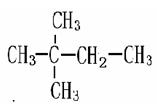
(10)
⑾3517Cl
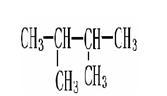
(12)
在一定条件下,1 mol某气体若被O2完全氧化放热98.0 kJ,现有2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为
(注:某反应物的转化率=该反应物转化(消耗)的物质的量÷该反应物起始的物质的量×100%)
Na3N是科学家制备的一种重要化合物,它与水作用可产生NH3,请回答:
(1)该化合物所形成的晶体类型属于________
(2)写出Na3N与水反应的化学方程式:_________________________________
(3)Na3N放入足量的盐酸中可以生成两种盐,其化学式分别为__________和__________
盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)△H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式: