A、B、C、W、X、Y、Z是由周期表中短周期元素组成的七种物质,其中A、B、C是三种固体单质,W、X、Y、Z是由两种元素组成的化合物。它们之间的转化关系如图所示(所有反应物和生成物均未在框图中: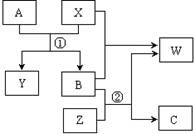
回答下列问题:
(1)化合物Z的晶体类型属于__________晶体。
(2)写出单质C的一种用途__________________________________。
(3)航天科技测知化合物N是金星大气层的成分之一,组成化合物N的元素与W相同。已知N中两种元素的质量之比为2:1,N的相对原子质量小于80,则N的化学式为_____________。又知该分子中的每个原子都满足最外层8电子的稳定结构,试写出其电子式_________________。
(4)写出下列反应的化学方程式:
①__________________________________;
②__________________________________。
(1)某反应池中,发生“生物硝化过程”,如果不考虑过程中硝化细菌的增殖,其净反应如下式所示: ①
①
配平上面化学方程式,将系数填入方框中。
②将铵态氮中的1 mg氮转化成硝酸根中的氮,需氧气多少毫克?
③为什么在反应中需要不断添加碱?
(2)3级反应池中发生的“生物反硝化过程”,通常需要外加甲醇,净反应如下所示: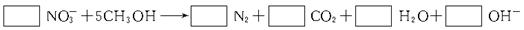
配平上面化学方程式,将系数填入方框中。
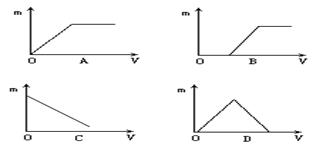
(1)在澄清石灰水中通入CO2,直至过量。
(2)在硫酸和盐酸混合溶液中滴加氢氧化钡溶液,直至过量。
(3)在碳酸钡的悬浊液中加盐酸,直至过量。
回答:(1)_______(2)________(3)________。
(1)写出上述两个反应的化学方程式:①_____________;②_________________。
(2)试说明用熟石灰的悬浊液,而不用澄清石灰水洗涤废气的理由:________。
(3)在英国进行的一个研究结果表明:高烟囱可以有效地降低地表面二氧化硫的浓度。在二十世纪六七十年代的10年间,由发电厂排放出的二氧化硫增加了35%,但由于建造高烟囱的结果使地面二氧化硫的浓度降低了30%之多。请从全球环境保护的角度,分析这种方法是否可取?答____________________。
(1)分析判断A和B 各是什么物质,写出各自的化学式。
(2)写出①~⑦各步反应的化学方程式。

2SO2(g)+O2(g) ≒2SO3(g);ΔH=-196.6KJ/mol
(1)该反应在__________(设备)中进行,这种生产硫酸的方法叫做________。
(2)在实际生产中,操作温度选定400∽500℃,这是因为______________。
(3)硫酸工业选定压强通常采用_____________,作出这种选择的依据是______________________________。