把A、B、C、D4块金属片浸入稀硫酸中,用导线两两相连组成原电池。若A、B相连时,A为负极;C、D相连时,D上产生大量气泡;A、C相连时,电流由C经导线流向A;B、D相连时,电子由D经导线流向B,则此4种金属的活动性由强到弱的顺序为( )
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>A>C>D
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)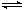 CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是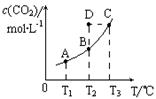
A.反应CO(g)+H2O(g)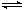 CO2(g)+H2(g)的△H>0 CO2(g)+H2(g)的△H>0 |
| B.在T2时,若反应进行到状态D,则一定有v正<v逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)小 |
| D.由D状态转变为C状态后,混合气体的平均相对分子质量不变 |
把3mol P和2.5mol Q置于2L密闭容器中,发生如下反应:3P(g)+Q(g)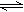 xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是
xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是
| A.5min内P的平均反应速率为0.15mol/(L·min) | B.Q的平衡浓度为1mol/L |
| C.Q的转化率为25% | D.x是2 |
如下图所示,两个连通容器用活塞分开,左右两室各充入一定量NO和O2,且恰好使两容器内气体密度相同,打开活塞,使NO与O2充分反应,最终容器内混合气体密度比原来
| A.减小 | B.增大 | C.不变 | D.无法确定 |
有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器压强恒定。在同温同压和等体积条件下,向a和b两容器中通入等物质的量的NO2,发生反应: 2NO2 N2O4△H<0,则以下说法正确的是
N2O4△H<0,则以下说法正确的是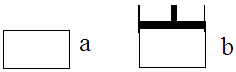
| A.反应起始时两容器的反应速率va和vb的关系:va<vb |
| B.反应过程中两容器内的反应速率va和vb的关系:va<vb |
| C.反应达到平衡时,两容器内压强相同 |
| D.反应达到平衡时,两容器的NO2的转化率相同 |
可逆反应A(g)+B C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是
| A.若B是气体,增大A的浓度会使B转化率增大 |
| B.若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体 |
| C.升高温度,C百分含量减少,说明正反应是放热反应 |
| D.增大压强,平衡不移动,说明B是气体 |