标准状况下,某同学向 100 mL H2S 饱和溶液中通入SO2, 所得溶液 pH 变化如图所示。下列分析中,正确的是( )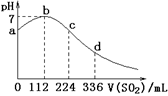
| A.ab 段反应是:SO2 + 2 H2S="3S↓+2" H2O |
| B.亚硫酸是比氢硫酸更弱的酸 |
| C.原H2S溶液的物质的量浓度为0.05 mol•L-1 |
| D.b 点对应的溶液导电性最强 |
在密闭容器中,一定量混合气体发生下列反应:aA(g)+bB(g)⇌cC(g)+dD(g),达到平衡后,测得C气体的浓度为0.5mol/L.当在恒温下,将密闭容器的体积缩小为1/2,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是
| A.反应速率降低 | B.平衡向右移动 | C.B的转化率提高 | D.a+b<c+d |
NH3加热分解为N2和H2,在相同条件下,测得分解后混合气体密度为分解前的2/3,则氨的分解率为
| A.80% | B.60% | C. 50% | D.40% |
pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是
| A.反应开始时的速率:甲>乙 |
| B.反应结束时,pH值:甲=乙 |
| C.反应开始时,酸的物质的量浓度:甲=乙 |
| D.反应所需时间:甲>乙 |
下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是
| A.2NO2(气)⇌N2O4(气) (正反应为放热反应) |
| B.C(固)+CO2(气)⇌2CO(气) (正反应为吸热反应) |
| C.N2(气)+3H2(气)⇌2NH3(气) (正反应为放热反应) |
| D.H2S(气)⇌H2(气)+S(固) (正反应为吸热反应) |
在一定条件下,发生CO+NO2⇌CO2+NO的反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是
| A.正反应为吸热反应 | B.正反应为放热反应 |
| C.降温后CO的浓度增大 | D.降温后各物质的浓度不变 |