下列实验操作不正确的是( )
①向盛有20mL沸腾蒸馏水的烧杯中滴加1mL~2mLFeCl3饱和溶液。继续煮沸至溶
液呈红褐色,得Fe(OH) 3胶体 ②配制FeCl3溶液时,将一定量氯化铁溶解在少量较浓的盐酸中,再用蒸馏水稀释到所需浓度 ③将氢氧化钠固体放在滤纸上称量 ④为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
| A.①② | B.②③ | C.③④ | D.①④ |
根据广州中心气象台报道,近年每到春季,我省沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞。雾属于下列分散系中的
| A.溶液 | B.悬浊液 | C.乳浊液 | D.胶体 |
下图表示的一些物质或概念间的从属关系中不正确的是

对于密闭容器中进行的反应:2NO2 N2O4,下列说法正确的是
N2O4,下列说法正确的是
| A.增大NO2的浓度,平衡常数增大 |
| B.增大N2O4的浓度,平衡常数增大 |
| C.增大NO2的浓度,正反应速率加快,逆反应速率减慢 |
| D.增大NO2的浓度,平衡常数不变 |
下列事实不能用勒沙特列原理解释的是
| A.用排饱和氯化钠溶液的方法收集氯气 |
| B.加催化剂,在一定条件下使N2和H2转化为NH3 |
| C.加压有利于SO2与O2反应生成SO3 |
| D.可用浓氨水和氢氧化钠固体来快速制取氨气 |
某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);ΔH <0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g);ΔH <0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是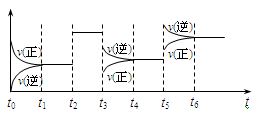
| A.t5时增大了压强 |
| B.t3时降低了温度 |
| C.t2时加入了催化剂 |
| D.t4~t5时间内转化率一定最低 |