具有一个羟基的有机物A与8g乙酸充分反应生成了10.2g酯,经分析还有2g乙酸剩余,下列有可能是A的为
| A.C2H5OH | B.C6H5-CH2-OH | C. |
D.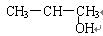 |
一定条件下,可逆反应N2(g)+3H2(g)  2NH3(g) ΔH<0,化学反应速率与反应时间的关系如右图所示。10秒内,c(H2)下降了0.75mol/L,下列说法不正确的是:
2NH3(g) ΔH<0,化学反应速率与反应时间的关系如右图所示。10秒内,c(H2)下降了0.75mol/L,下列说法不正确的是: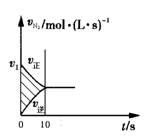
| A.图中v1大于0.05 mol/(L·s) |
| B.氢气的起始瞬时速率为0.075mol/(L·s) |
| C.10秒内氨气的平均速率为0.05mol/(L·s) |
| D.其他条件不变,升高温度,v1增大,阴影面积减少 |
把a L含(NH4)2SO4和NH4NO3的混合液分为两等份:一份加入bmol 烧碱并加热,恰好把NH3全部赶出,另一份需含c molBaCl2溶液,使沉淀反应刚好完全,则NO3ˉ的浓度是
A. mol/L mol/L |
B.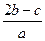 mol/L mol/L |
C. mol/L mol/L |
D. mol/L mol/L |
2007年10月,一台湾女孩因食用河虾后服用大剂量的维生素C而中毒。菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有+5价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷。下列说法正确的是
| A.在该反应中维生素C作催化剂 |
| B.因为河虾中含有砷元素,所以不能食用 |
| C.砒霜是砷的氧化物,由上述信息可推知砒霜中含有的砷是+3价 |
| D.上述反应中维生素C作氧化剂 |
用Na2SO3还原MnO4-,如果还原含有2.4×10-3molMnO4-的溶液时,消耗30mL0.2mol/LNa2SO3溶液,则Mn元素在还原产物中的化合价是
| A.+1 | B.+2 | C.+4 | D.+5 |
下列溶液中Cl-浓度与50 mL 1 mol·L-1NaCl溶液中Cl-浓度相等的是
| A.150 mL 1 mol·L-1的NaCl溶液 | B.50 mL 2 mol·L-1 NH4Cl溶液 |
| C.150 mL 1 mol·L-1的KCl溶液 | D.50 mL 1 mol·L-1的FeCl3溶液 |