右图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是( )
| A.H2S | B.HCl | C.PH3 | D.SiH4 |
向含Fe(NO3)3、Cu(NO3)2、HNO3的稀溶液中逐渐加入铁粉, 的变化如图所示。下列离子方程式错误的是( )
的变化如图所示。下列离子方程式错误的是( )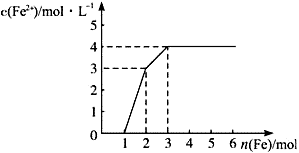
| A.0~1 : Fe+ NO3—+4H+=Fe3++ NO↑+2H2O | B.1~2 : Fe+2Fe3+ =3Fe2+ |
| C.2~3 : Fe+Cu2+=Fe2++Cu | D.0~3 : 3Fe+2Fe3++2Cu2+ =5Fe2++2Cu |
某溶液中除H+、OH—外,还含有大量的Mg2+、Fe3+、Cl—,且这三种离子的物质的量浓度之比为1:1:6。下列有关该溶液的判断正确的是()
| A.向该溶液中加入KI溶液后,原有的五种离子的物质的量不变 |
| B.向该溶液中滴加稀NaOH溶液,立即出现白色沉淀 |
| C.若溶液中c(Cl—) =" 0.6" mol/L,则该溶液的pH为1 |
| D.向该溶液中加入过量铁粉,只发生置换反应 |
加热一定量的 碳酸氢钠固体至200℃,将产生的全部气体用足量的过氧化钠粉末完全吸收得到固体M,取一定量的固体M与V mL C mol·L—
碳酸氢钠固体至200℃,将产生的全部气体用足量的过氧化钠粉末完全吸收得到固体M,取一定量的固体M与V mL C mol·L— 1盐酸恰好完全反应得到中性溶液和混合气体X,则混合气体X的物质的量为(不考虑溶液中溶解气体) ( )
1盐酸恰好完全反应得到中性溶液和混合气体X,则混合气体X的物质的量为(不考虑溶液中溶解气体) ( )
A.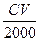 mol mol |
B.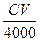 mol mol |
C.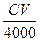 mol<n(X)< mol<n(X)<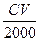 mol mol |
D.无法计算 |
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是()
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
| A.只有①④ | B.只有③ | C.只有②③ | D.只有①③④ |
某溶液中含有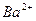 、
、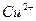 、
、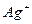 ,现用
,现用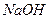 溶液、盐酸和
溶液、盐酸和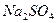 溶液将这三种离子逐一沉淀分离,其流程如下图所示。
溶液将这三种离子逐一沉淀分离,其流程如下图所示。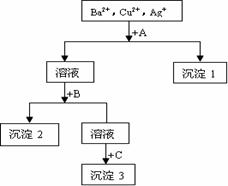
下列说法正确的是()
A.试剂A为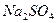 溶液 溶液 |
B.沉淀3的化学式可能是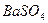 |
C.生成沉淀1的离子方程式为: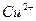 +2 +2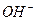 = = 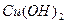 ↓ ↓ |
D.生成沉淀2的离子方程式为 : :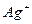 + +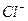 = =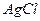 ↓ ↓ |