已知A—L所代表的物质(溶液中的溶质),除B外均是中学化学里常见的物质,它们的转化关系如图所示。(反应时加入或生成水均略去)
已知:a.通常状况下,A是淡黄色固体,C是红棕色固体,D是气体单质,E是无色无味气体;b.反应②—③是工业生产L的部分反应,反应④是工业生产普通玻璃的反应之一;c.B是由两种元素组成的化合物,其质量比为7:5;请填写下列空白: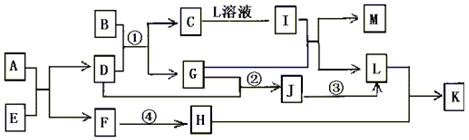
(1)A的电子式 ,B的化学式 。
(2)反应②的工业生产条件 ,写出工业生产L时反应①的设备名称 。
(3)完成下列反应方程式:
①I+G→M+L的离子方程式: ,
②反应④的化学方程式: 。
按要求填空:
(1)含有相同氧原子数的CO2和CO:物质的量之比为___________;质量之比为______________。
(2)写出除去FeCl3溶液中的FeCl2所需的试剂:_______________(填化学式)
(3)海水的溴以Br-的形式存在,海水中提溴的方法通常是:向苦卤中通入Cl2是为了提取Br2,为
大量富集Br2,常先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收,该反应的离子方程式是 。
钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式: 。
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3•xH2O),写出铁发生电化学腐蚀时正极的电极反应: 。
(3)下列哪个装置可防止铁棒被腐蚀 (填字母)。

(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如右图,请回答:
① B电极对应的金属是 (写元素名称),A电极的电极反应式是 。
② 若电镀前两电极的质量相同,电镀完成后, 若电镀时电路中通过的电子为0.2mol,将它们取出洗净、烘干、称量,则A、B两极质量相差 g。
用石墨电极电解500 mL含一种溶质的某蓝色溶液,如右图所示,观察到A极表面有红色固体物质生成,B极上有无色气体生成;当溶液中的原有溶质完全电解后,取出A极,洗涤、干燥、称量,电极增重1.6 g,回答下列问题:
(1)B电极发生反应的电极反应式_______________________。
(2)写出电解时反应的离子方程式______________________________。
(3)电解后溶液中H+物质的量浓度为________________,要使电解后溶液恢复到电解前的状态,则需加入____________,其质量为________________。(假设电解前后溶液的体积不变)
(4)原溶液可能是________________溶液。
(1)已知:①C3H8(g)+5O2(g)==3CO2(g)+4H2O(l) ΔH="-2220.0" kJ·mol-1
②H2O(l)==H2O(g) ΔH="+44.0" kJ·mol-1
写出丙烷燃烧生成CO2和气态水的热化学方程式:______________________。
(2)航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。我国发射的“神舟五号”载人飞船是采用先进的甲烷电池为电能来源,该电池以KOH溶液为电解质。试回答:
①负极上的电极反应为________________________________;
②消耗标准状况下的5.6 L O2时,有________mol电子发生转移。
③开始放电时,正极附近溶液的pH________(填“增大”“减小”或“不变”)。
(1)质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是 。
(2)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是_________。(填序号)
① NaAlO2 ② Ca(OH)2③Na2CO3④Al(OH)3
(3)Na、Mg、Al分别与足量的硫酸溶液反应,当生成气体的质量相同时,消耗掉的Na、Mg、Al的物质的量之比为______________。
(4)足量的Al分别与等浓度的硫酸溶液、氢氧化钠溶液反应,当生成气体的质量相同时,硫酸溶液和氢氧化钠溶液的体积比为______________。