下列离子方程式正确的是
| A.向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O=Fe(OH)3↓+3H+ |
| B.碳酸氢镁溶液中加入足量的氢氧化钠溶液:Mg2++2HCO3-+2OH-=MgCO3↓+CO32-+2H2O |
| C.硝酸铝溶液中加入过量的氨水:Al3++4NH3+2H2O====AlO2-+4NH4+ |
| D.淀粉碘化钾试纸在潮湿空气中变蓝:4I-+O2+2H2O====2I2+4OH- |
学习时通过比较、归纳,可以加深对问题的认识。下列比较或归纳一定正确的是
| A.稳定性:NH3<PH3<AsH3 | B.离子半径:阴离子>阳离子 |
| C.酸性:H2SO4>H3PO4>H2SiO3 | D.熔沸点:离子化合物>共价化合物 |
某化学兴趣小组设计如图原电池:其中a、b分别为Cu和Ag,甲和乙分别是氨水和硝酸银溶液,盐桥的琼脂中吸附有KCl溶液,反应一段时间后,下列说法正确的是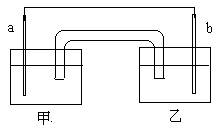
| A.b为负极,电极方程式为:Ag + + e- =" Ag" | B.甲中出现大量蓝色沉淀 |
| C.总反应为:Cu + 2 Ag + = Cu2+ + Ag | D.反应时,盐桥中的K+向乙方向移动 |
设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有
① 0.25molNa2O2中含有的阴离子数为0.5 NA
②0.05 mol熔融的KHSO4中含有阳离子数目为0.10 NA
③ 1mol α-氨基乙酸(甘氨酸)分子中存在10NA对共用电子
④ 1mol/L的Na2CO3溶液中含有CO32-一定小于NA⑤ 标准状况下,2.24L CHCl3含有的分子数为0.1 NA
⑥电解精炼铜时,当阳极溶解32 g铜时,转移的电子数为NA个
⑦ 2mol的Zn与足量的浓硫酸反应转移的电子数为4NA
| A.2个 | B.3个 | C.4个 | D.5个 |
若以M表示水的摩尔质量,V表示在标准状况下水蒸气的摩尔体积,ρ为在标准状况下的密度,NA为阿伏加德罗常数,m、Vx分别表示每个水分子的质量和体积,下面是四个关系式:①NA=Vρ/m,②ρ=M/(NAVx),③ m=M/NA,④Vx=V/NA,其中
| A.①②是正确的 | B.①③是正确的 |
| C.①③④是正确的 | D.①②③④都正确 |
下列描述,其因果关系成立的是
| A.因为NH3的水溶液可以导电,所以NH3是电解质 |
| B.因为SO2可以使溴水褪色,所以SO2具有漂白性 |
| C.因为某碱性溶液的焰色呈黄色,所以其溶质为NaOH |
| D.因为电解质溶于水后电离为离子,所以电解质在溶液中的反应实质是离子反应 |