100℃时,将0.1molN2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 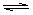 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是 ①烧瓶内气体的颜色不再加深; ②N2O4的消耗速率与NO2的生成速率之比为1∶2; ③NO2的生成速率与NO2消耗速率相等; ④NO2的物质的量浓度不变; ⑤烧瓶内气体的质量不再变化; ⑥烧瓶内气体的压强不再变化; ⑦烧瓶内气体的密度不再变化; ⑧烧瓶内气体的平均相对分子质量不再变化
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是 ①烧瓶内气体的颜色不再加深; ②N2O4的消耗速率与NO2的生成速率之比为1∶2; ③NO2的生成速率与NO2消耗速率相等; ④NO2的物质的量浓度不变; ⑤烧瓶内气体的质量不再变化; ⑥烧瓶内气体的压强不再变化; ⑦烧瓶内气体的密度不再变化; ⑧烧瓶内气体的平均相对分子质量不再变化
| A.②⑤⑦ | B.①③④⑥⑧ | C.只有③ | D.只有⑤ |
下列各溶液中,Na+物质的量浓度最大的是 ( )
| A.4L 0.5mol/LNaCl溶液 | B.1L 0.3mol/LNa2SO4溶液 |
| C.5L 0.4mol/LnaOH溶液 | D.2L 0.15mol/LNa3PO4溶液 |
下列说法正确的是()
| A.1mol·L-1的氯化钠溶液是指此溶液中含有1molNaCl |
| B.从1L0.5mol·L-1的NaCl溶液中取出100mL溶液,其物质的量浓度变为0.1mol·L-1 |
| C.500mL 0.2mol/L BaCl2溶液中Cl-离子总数为0.2NA |
| D.500mL 0.2mol/L BaCl2溶液中阴阳离子总数为0.4NA |
用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A.0.1 mol OH-含有NA个氧原子 |
| B.常温常压下,64 g SO2含有的的原子数为3NA |
| C.常温常压下, NA个CO2分子的体积大于22.4L |
| D.氯化氢气体的摩尔质量在数值上等于NA个氯化氢分子的质量之和 |
在标准状况下,如果1.6L氧气含a个氧分子,则阿伏加德罗常数的数值为( )
| A.28a | B.14a | C.a/28 | D.a/14 |
下列各组物质中,所含分子数一定相同的是( )
A 1g O2和 1g O3 B 0.2mol H2和 4.48 L Ne
C 1250C、1.01× 105Pa时,20 L H2和 20 L O2
D 常温常压下44g CO2和 6.02×1022个O2分子