节能减排,作为我国“十一五”规划中一重要任务,已不仅是政府的一个行动目标,而且还能给企业带来经营上的收入,让城市居民能获得一个较好的生存环境。节能减排更是一个人类解决环境问题的必经之路。下列措施和节能减排无关的是
| A.将白炽灯换成节能灯 | B.发展利用新能源,如太阳能、氢能、核能等 |
| C.大力植树造林,增加绿色植被 | D.少开汽车,采取骑自行车或做公交车 |
某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO3-,现取两份100mL溶液进行如下实验:已知HNO2是一种不稳定的弱酸,易分解生成NO2和NO,AgNO2是一种不溶于水的白色沉淀。
①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol·L-1的硫酸溶液恰好完全吸收,酸也不剩余。根据上述实验,以下推测不正确的是
| A.原溶液一定不存在较大浓度的H+、Mg2+ |
| B.原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1 |
| C.不能确定原溶液是否含有K+、NO3- |
| D.实验中产生的棕色气体遇空气颜色会加深 |
常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8。已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法不正确的是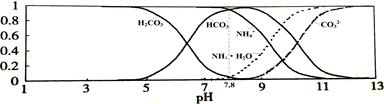
| A.NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3·H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B.往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 |
| C.通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3) |
| D.当溶液的pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3·H2O)>c(CO32-) |
如图是可逆反应A+2B 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应
D.A、B、C、D均为气体
下图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液。下列说法不正确的是

| A.甲中铜片作阴极,K+向铜片电极移动 |
B.乙中正极发生的电极反应为CO2+6e-+6H+ CH3OH+H2O CH3OH+H2O |
| C.乙中H2SO4的作用是增强溶液的导电性 |
| D.甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 |
下列说法正确的是
| A.增大压强任何反应的反应速率都一定增大 |
B.已知H2CO3的电离常数分别为Ka1=4.3×10-7、Ka2=5.61×10-11,苯酚的电离常数Ka=1.1×10-10。苯酚钠溶液中通入少量CO2时的化学方程式为: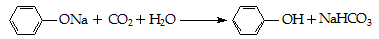 |
| C.pH=2的盐酸和pH=4的硫酸溶液等体积混合后溶液的pH=3 |
| D.在滴有酚酞的氢氧化钠溶液中逐滴滴入盐酸至红色恰好消失,此时溶液的pH=7 |