NA代表阿伏加德罗常数的值,下列说法正确的是
| A.5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA个 |
| B.标准状况下,2.24 L水中含有0.1 NA个水分子 |
| C.1.12 L氯气中含有0.1 NA个氯原子 |
| D.12 g 石墨和金刚石的混合固体中,含碳原子NA个 |
下列实验设计能够成功的是
| A.检验亚硫酸钠试样是否变质: 试样 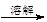 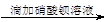 白色沉淀 白色沉淀 沉淀不溶解→说明试样已变质 沉淀不溶解→说明试样已变质 |
| B.除去粗盐中含有的硫酸钙杂质 粗盐 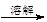 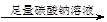     精盐 精盐 |
| C.检验某溶液中是否含有Fe2+ 试样  溶液颜色无变化 溶液颜色无变化 溶液变红色→溶液中含有Fe2+ 溶液变红色→溶液中含有Fe2+ |
| D.证明酸性条件H2O2的氧化性比I2强: |
NaI溶液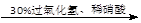
 溶液变紫色→氧化性:H2O2>I2
溶液变紫色→氧化性:H2O2>I2
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法不正确的是
| A.原子半径大小顺序:r(Z)>r(W)>r(X)>r(Y) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应水化物的酸性比W的强 |
| D.Y的气态简单氢化物的热稳定性比W的强 |
下列离子方程式的书写正确的是
| A.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O |
| B.向0.1L 5mol/L亚硫酸氢铵溶液中逐滴加入0.1L 7 mol·L-1 NaOH溶液: 2NH4++5HSO3-+7OH-=2NH3·H2O+5SO32-+5H2O |
| C.FeI2溶液中通入过量Cl2:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
下列叙述或离子方程式书写正确的是
| A.将少量二氧化硫通入次氯酸钠溶液中:SO2+H2O+3ClO-=SO42-+Cl-+2HClO |
| B.用氨水溶解氯化银沉淀:Ag++2 NH3·H2O=[Ag(NH3)2]++2H2O |
C.用惰性电极电解MgCl2溶液:2Cl-+ 2H2O Cl2↑+ H2↑+ 2OH- Cl2↑+ H2↑+ 2OH- |
| D.等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应:Ba2++2OH-+2NH4++SO42-= BaSO4↓+2NH3·H2O |
下列有关实验装置进行的相应实验,能达到实验目的的是
| A.图①除去CO2中的HCl |
| B.图②装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.图③所示装置制取并收集干燥纯净的NH3 |
| D.图④证明CH3CH2OH发生消去反应生成了乙烯 |