已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是( )
A.上述实验证明氧化性:MnO >Cl2>Fe3+>I2 >Cl2>Fe3+>I2 |
| B.实验①证明Cl—被还原 |
| C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D.实验③中氧化剂与还原剂的物质的量之比为2:1 |
甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合下图。其中甲和X不可能是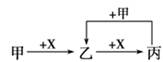
| A.甲为NaOH溶液、X为AlCl3溶液 |
| B.甲为H2S、X为O2 |
| C.甲为Fe、X为Cl2 |
| D.甲为SO2、X为NaOH溶液 |
下列实验能达到预期目的的是
| 选项 |
实验 |
实验目的或结论 |
| A |
向某溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解,证明该溶液中存在AlO2- |
Al(OH)3是两性氢氧化物,不溶于碳酸溶液 |
| B |
将某气体通入品红溶液,溶液褪色 |
检验气体中的SO2 |
| C |
测定等物质的量浓度的HCOOK和K2S溶液的pH |
比较Ka(HCOOH)和Ka2(H2S)的大小 |
| D |
向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4溶液和KMnO4溶液,观察气体产生的速度 |
比较CuSO4和KMnO4的催化效果 |
下列关于有机化合物的结构、性质说法正确的是
| A.乙酸、乙酸乙酯都可和NaOH溶液发生中和反应 |
| B.苯分子中的碳碳键不同于乙烯分子中的碳碳双键,因此苯不能发生加成反应 |
| C.用新制氢氧化铜悬浊液可以鉴别乙酸、葡萄糖和淀粉三种溶液 |
| D.正丁烷和异丁烷的一氯取代物都只有两种,它们的密度也相同 |
下列有关物质应用的说法正确的是
| A.明矾在自来水的生产过程中,常用于净水及杀菌消毒 |
| B.铁红常用作红色油漆和涂料 |
| C.碳酸钠在医疗上是治疗胃酸过多的一种药剂 |
| D.食品包装袋、食物保鲜膜等材料的主要成份是聚氯乙烯 |
硼氢化物作为一种液体燃料,具有便于储存、运输等特点,且其活性要远高于醇类物质。一种以NaBH4为燃料的电池在一些特殊领域如水下和航天方面的便携式电源获得应用,该电池用双氧水作为氧化剂,NaOH溶液作为电解质溶液。该电池的装置图如图所示,下列关于该电池的叙述不正确的是
| A.a电极发生氧化反应 |
| B.b极电极反应式:H2O2+2e-=2OH- |
| C.放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4 |
| D.其中的离子交换膜需选用阳离子交换膜 |