配制100 mL 1 mol·L-1氢氧化钠溶液,下列操作错误的是( )
| A.在托盘天平上放两片大小、质量一样的纸,然后将氢氧化钠放在纸片上进行称量 |
| B.把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液移入容量瓶中 |
| C.用蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液也移入容量瓶中 |
D.沿着玻璃棒往容量瓶中加入蒸馏水, 到离刻度线1~2cm时改用胶头滴管滴加,直到溶液凹面恰好与刻度相切 到离刻度线1~2cm时改用胶头滴管滴加,直到溶液凹面恰好与刻度相切 |
高铁酸钾 (K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。
湿法制备的主要反应方程为:2Fe(OH)3 +3ClO-+4OH- =2FeO42- +3Cl- +5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
下列有关说法不正确的是:()
| A.高铁酸钾中铁显+6价 |
| B.湿法中每生成1mol Na2FeO4转移3mol电子 |
| C.干法中每生成1 mol Na2FeO4转移4mol电子 |
| D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质 |
下面关于电解质电离的叙述正确的是()
| A.CaCO3在水中溶解度很小,其导电能力很弱,所以 CaCO3是弱电解质 |
| B.CaCO3在水中溶解度很小,但溶解的 CaCO3全部电离,所以 CaCO3是强电解质 |
| C.氯气和氨气的水溶液导电性都很好,所以它们是强电解质 |
| D.水难电离,纯水几乎不导电,水是非电解质 |
1.以下对化学反应知识的归纳和总结中,正确的是()
| A.酸跟活泼金属反应一定生成盐和氢气 | B.碱能跟一切非金属氧化物反应 |
| C.单质和化合物的反应一定是置换反 | D.置换反应不一定要在溶液中进行 |
在氢氧化钾溶液中,已知钾离子与水分子的物质的量之比为a : b,溶液的密度为d g/cm3,则溶液的浓度为 ( )
|
A.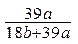 ×100% ×100% |
B.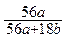 % % |
C.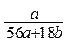 mol/L mol/L |
D.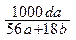 mol/L mol/L |
下列说法正确的是()
| A.PH=0的溶液中,K+、I-、SO42-、Cl-可以大量共存 |
| B.在无色溶液中,Na+、Fe3+、HCO3-、NO3-可以大量共存 |
C.在显中性的水溶液中,c(OH-)不一定等于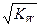 |
| D.纯水的PH一定等于7 |