向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加等体积水稀释时,都会引起( )
| A.溶液的pH增大 | B.CH3COOH的电离程度增大 |
| C.溶液的导电能力减小 | D.溶液的c (OH – )减小 |
下列有机物中,含有两种官能团的是
| A.CH2=CH-CH2 Br | B.CH≡CH |
| C.Cl-C2H4-Cl | D.Br-CH= CH-Cl |
下列化合物的性质属于羟基对苯环影响的是
| A.苯酚溶液显弱酸性 |
| B.苯酚比苯容易发生溴代反应 |
| C.苯酚能与NaOH溶液反应,而苯甲醇不能与NaOH溶液反应 |
| D.苯酚和乙醇在60℃的水浴中,分别加入金属钠,苯酚中明显反应剧烈 |
下列有机物命名正确的是
| A.2-乙基丁烷 |
| B.2-乙基1-丁烯 |
C.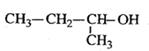 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D.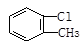 间氯甲苯 间氯甲苯 |
下列有关化学用语表示正确的是
| A.乙烯的结构简式:CH2CH2 |
B.对甲基苯酚的结构简式: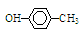 |
C.3,3—二甲基—1—戊烯的键线式: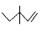 |
D.乙醇分子的比例模型: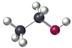 |
下列物质中属于有机物的是
| A.碳酸 | B.二氧化碳 | C.煤 | D.甲烷 |