一定温度下将amolPCl5通入一个容积不变的反应器中,达到如下平衡:PCl5 PCl3+Cl2测得压强为P1,此时向反应器中再通入amolPCl5,在温度不变的情况下再度达到平衡,测得压强为P2。则P1和P2的关系是( )
PCl3+Cl2测得压强为P1,此时向反应器中再通入amolPCl5,在温度不变的情况下再度达到平衡,测得压强为P2。则P1和P2的关系是( )
| A.2P1>P2 | B.2P1=P2 | C.2P1<P2 | D.无法判断 |
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
A.N2电子式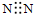 |
B.Cl原子的结构示意图为 |
| C.CO2的结构式为:O=C=O | D.质量数为37的氯原子为 Cl Cl |
下列关于浓HNO3与浓H2SO4的叙述正确的是
| A.常温下都不可用铁制容器贮存 | B.常温下都能与铜较快反应 |
| C.露置于空气中,溶液质量均减轻 | D.露置于空气中,溶液浓度均降低 |
在10℃时某化学反应速率为0.1mol/(L·s),若温度每升高10℃反应速率增加到原来的2倍。为了把该反应速率提高到1.6 mol/(L·s),则该反应需在什么温度下进行()
| A.30℃ | B.40℃ | C.50℃ | D.60℃ |
实验室用4 mol SO2与2 mol O2在一定条件下进行下列反应:2SO2(g)+O2(g)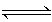 2SO3(g)ΔH ="-196.64" kJ/mol,当放出314.624 kJ热量时,SO2的转化率为()
2SO3(g)ΔH ="-196.64" kJ/mol,当放出314.624 kJ热量时,SO2的转化率为()
| A.40% | B.50% | C.80% | D.90% |
管道煤气的主要成分是H2、CO和少量的甲烷。相应的热化学反应方程式为:
2H2(g)+O2(g)==2H2O(l)ΔH ="-571.6" kJ/mol
2CO(g)+O2(g)==2CO2(g)ΔH ="-566" kJ/mol
CH4(g)+2O2(g)==CO2(g)+2H2O(l)ΔH="-890.3" kJ/mol
当使用管道煤气的用户改用天然气后,在相同条件下燃烧等体积的燃气,理论上所获得的热值后者大约是前者的多少倍()
| A.0.8 | B.1.3 | C.1.6 | D.3.1 |