硫酸在国民经济中占有极其重要的地位,下图是工业接触法制硫酸的简单流程图,试回答下列有关问题.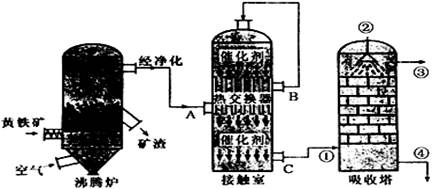
(1)在实际生产过程中,进入接触室的气体中O2的体积分数是SO2体积分数的1.5倍,其原因是
(2)在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室。按此密闭体系中气体的流向,则在B处流出的气体(除N2外)为 ;
(3)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N2 82%):
| 压强/MPa 温度/℃ |
0.1 |
0.5 |
1 |
10 |
| 400 |
99.2% |
99.6% |
99.7% |
99.9% |
| 500 |
93.5% |
96.9% |
97.8% |
99.3% |
| 600 |
73.7% |
85.8% |
89.5% |
96.4% |
①已知SO2的氧化是放热反应,如何利用表中数据推断此结论?
;
②在400-500℃时,SO2的催化氧化采用常压而不是高压,主要原因是: ;
(4)选择适应的催化剂,是否可以提高SO2的转化率? ;是否可以增大该反应所放出的热量? (填“是” 或“否”);
(5)若用浓硫酸吸收SO3可以得到H2SO4·SO3。用1000g 98 % 的H2SO4充分吸收SO3后,再进行稀释,可以得到98% 的硫酸的质量是 。
反应A+3B=2C+2D在四种不同情况下的反应速率可分别为
①v
| A.=0.15 mol/(L·s) ②v | B.=0.6 mol/(L·s) ③v | C.=0.4 mol/(L·s) ④v | D.=0.45 mol/(L·s) |
该反应进行的快慢顺序为________。
化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下列相关说法正确的是________(填序号)。
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提上日程,其首要原因是电池外壳的金属材料需要回收
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应式可表示为2Ni(OH)2+Cd(OH)2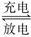 Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O
已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是________(填序号)。
A.以上反应是可逆反应
B.反应环境为碱性
C.电池放电时Cd作负极
D.该电池是一种二次电池
(3)在宇宙飞船和其他航天器上经常使用的氢氧燃料电池是一种新型电源,其构造如图所示:a、b两个电极均由多孔的碳块组成,通入的氢气和氧气由孔隙中逸入,并在电极表面发生反应而放电。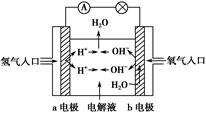
①a电极是电源的________极;
②若该电池为飞行员提供了360 kg的水,则电路中通过了________mol电子。
铅蓄电池是典型的可充电电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO42—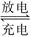 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
放电时:正极的电极反应式是______________________________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加________g。
如下图所示,可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式〔当电解质溶液为NaOH(aq)或KOH(aq)时〕两种。试回答下列问题: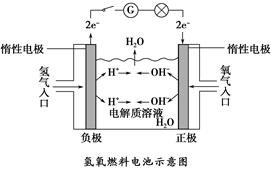
(1)酸式电池的电极反应:负极_______________,正极______________;电池总反应:________________;
电解质溶液pH的变化________(填“变大”“变小”或“不变”)。
(2)碱式电池的电极反应:负极_________________,正极_________________;电池总反应:______________;电解质溶液pH的变化________(填“变大”“变小”或“不变”)。
燃料电池是目前正在探索的一种新型电池。它主要是利用燃料在燃烧过程中把化学能直接转化为电能,目前已经使用的氢氧燃料电池的基本反应是
x极:O2(气)+2H2O(液)+4e-=4OH-
y极:H2(气)+2OH--2e-=2H2O(液)
回答下列问题:
(1)x是________极,发生________反应。(填“氧化”或“还原”,下同)
(2)y是________极,发生________反应。
总反应方程式为______________________。
(3)若反应后得到5.4 g液态水,此时氢氧燃料电池转移的电子数为________。