下列离子方程式书写正确的是( )
| A.氯气和水的反应: C12+H2O=2H++C1-+ClO- |
| B.稀硝酸与过量的铁屑反应: 3Fe+8H++2NO3- = 3Fe3++2NO↑+4H2O |
| C.铝跟氢氧化钠溶液反应:2Al + 2H2O + 2OH-=" 2" AlO2-+ 3H2↑ |
D.三氯化铁浓溶液滴入沸水中,制取氢氧化铁胶体: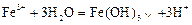 |
若aAm+与bBn-的核外电子排布相同,则下列关系不正确的是
A.a =" b+" m + n B.离子半径Am+<Bn-
C.原子半径A>BD.A、B一定都是短周期元素
下列有关实验现象的描述正确的是
| A.乙炔燃烧时火焰明亮并伴有黑烟 |
| B.在苯和甲苯中分别滴加几滴高锰酸钾酸性溶液振荡,高锰酸钾酸性溶液均褪色 |
| C.在乙醇中加入黄豆粒大小的金属钠,钠浮在液面上,熔化成光亮的小球,反应剧烈而迅速消失 |
| D.在溴乙烷和氢氧化钠溶液共热后的溶液中,加几滴硝酸银溶液产生淡黄色沉淀 |
下列反应:(I)1—溴丙烷与2—溴丙烷分别和氢氧化钠醇溶液混合加热
(II)1—溴丙烷与2—溴丙烷分别和氢氧化钠水溶液混合加热,关于反应中生成的有机物的说法中正确的是
| A.(I)和(II)产物均不同 | B.(I)和(II)产物均相同 |
| C.(I)产物相同,(II)产物不同 | D.(I)产物不同,(II)产物相同 |
下列说法中不正确的是
| A.质谱、红外光谱、核磁共振氢谱均为鉴定有机物结构的化学方法 |
| B.目前有许多测定相对分子质量的方法,质谱法是最精确、快捷的方法 |
| C.从红外光谱图中可以获得分子中含有何种化学键或官能团的信息 |
| D.从核磁共振氢谱图上可以推知有机物分子中有几种不同类型的氢原子及它们的数目 |
构成下列物质的粒子中所含化学键的类型和该固态物质晶体类型均相同的是
| A.HCl和NaCl | B.CO2和SiO2 | C.CH4和CCl4 | D.Na2O2和H2O2 |