图表法、图象法是常用的科学研究方法
I.短周期某主族元素M的电离能情况如图(A)所示。则M元素位于周期表的第 族。
II.图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是: ,理由是:
。
CH4、NH3、H2O、HF四种氢化物的沸点从高到低的顺序: > > > 。
III.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属则被科学家预测为是钛(Ti)。钛被誉为“未来世纪的金属”。试回答下列问题:
(1)22Ti元素基态原子的外围电子排布式为 。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,是很好的压电材料。偏钛酸钡晶体中晶胞的结构示意图如上图,则它的化学式是 ;每个氧离子周围的钛离子的配位数为 ,每个钡离子周围的氧离子配位数位为 。
饱和亚硫酸溶液的pKa(电离平衡常数的负对数,即pKa=-lgKa)数据如下: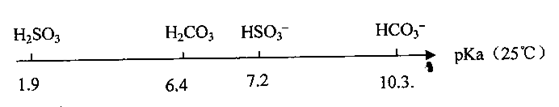
(1)比较H2SO3的Ka1和HSO3-的Ka2,Ka1Ka2(填‘‘>”、“<’’或“=”,下同)
(2)0.01 m ol.L-1NaHSO3溶液的pH=bl,0.01 tml·L-1NaHCO3溶液的pH=b2,
b1b2
(3)向10 mL 0.01 mol·L-1的H2SO3溶液中,滴加0.0l mol·L-1KOH溶液V(mL),
①当V="10" mL时,溶液中存在:c(K+)>c(HSO3-)>c(SO32-)>c(H2SO3),则c(H+)c(OH-)
②当V="a" mL时,溶液中离子浓度有如下关系:c(K+)=2c(SO32-)+c(HSO3-);当V="b" mL时,溶液中离子浓度有如下关系:c(K+)=c(SO32-)+c(HSO3--)+c(H2SO3);则a b。
(4)已知25℃时,Ksp(BaSO4)=1×10-10,将0.1 gBaSO4沉淀,分别用100mL蒸馏水和100mL 0.01mo1.L-1H2SO4溶液洗涤,两种洗涤方法中BaSO4沉淀的损耗量之比为.
天然气的主要成分是甲烷。在某平衡体系中存在CH4、H2O、CO、H2四种气体,
其平衡常数表达式为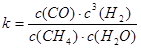 。已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷转化反应的影响如下图:
。已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷转化反应的影响如下图: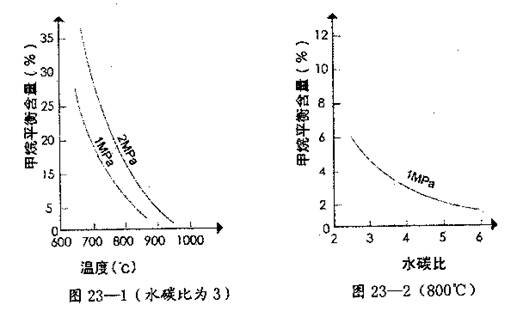
请回答下列问题:
(1)写出该可逆反应的化学方程式:
(2)根据图23—1判断△H0,△S0(选填“>”、“<”或“=”)。
(3)假设上述反应在恒容、恒温下进行,判断反应达到平衡状态时的标志是
| A.CO减少的化学反应速率和H2O(曲减少的化学反应速率相等 |
| B.CO、H2O(g)、CH4、H2的浓度都相等 |
| C.CO、H20(g)、CH4、H2的浓度都不再发生变化 |
| D.正、逆反应速率都为零 |
(4)在图23—2中画出压强为2 MPa时,CH4平衡含量与水碳比之间关系曲线。
各物质之间的转换关系如下图,部分生成物省略。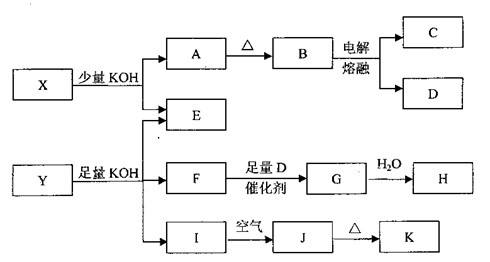
已知:①常温下,D、F、G为气体;C是日常生活中的常见金属;
②K的应用十分广泛,作为红色颜料跟某些油料混合,可以制成防锈油漆;
③E的水溶液中加盐酸无明显现象,然后加入BaCl2溶液出现浑浊。
请回答下列问题:
(1)写出F的电子式:;
(2)写出化学式:X、Y;
(3)写出C与KOH液反应的化学方程式:;写出H的稀溶液与I反应的离子方程式:;
有X、Y、z、w四种短周期元素,原子序数依次增大,其核电荷数总和为38。Y元素原子最外层电子数占核外总电子数的3/4;W元素原子最外层电子数比同周期Z元素原子最外层电子数多5个电子;W和 Y不属于同一主族。
(1)画出Y原子结构示意图:;
(2)从化合价角度分析,X元素可以排在周期表中I A、VIIA和族;
(3)Z、W两种元素最高价氧化物对应水化合物相互反应的化学方程式:;
(4)已知X2单质的热值为143 kJ·g-1,试写出X2单质在Y2单质中燃烧的热化学方程式:.
已知A、B、C、D、E、F、G、H 可以发生如下图所示的转化,反应中部分生成物已略去。其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。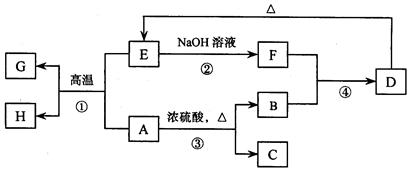
请填空:
(1)H的名称是。
(2)E的两种用途是、。
(3)反应③的化学方程式是。
(4)反应④的离子方程式是。